题目内容
表是元素周期表的一部分.根据表中10种元素,用元素符号或化学式填空.
(1)在 ①~⑩元素中金属性最强的金属元素是 ;
(2)在 ①~⑥元素所形成的气态氢化物中最不稳定的分子式是 ;
(3)在 ①~⑩元素中单质化学性质最稳定的原子结构示意图为 ;
(4)在 ①~⑩元素的最高价氧化物的水化物中酸性最强的分子式是 ;
(5)⑤、⑥、⑧、⑨所形成的离子中,半径最大的是 ;
(6)⑨和⑩的原子序数之差为 .
(7)⑩生成两种常见氧化物,它们的分子式是 和 .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ | ⑩ |
(2)在 ①~⑥元素所形成的气态氢化物中最不稳定的分子式是
(3)在 ①~⑩元素中单质化学性质最稳定的原子结构示意图为
(4)在 ①~⑩元素的最高价氧化物的水化物中酸性最强的分子式是
(5)⑤、⑥、⑧、⑨所形成的离子中,半径最大的是
(6)⑨和⑩的原子序数之差为
(7)⑩生成两种常见氧化物,它们的分子式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知①为C、②为O、③为Al、④为Si、⑤为S、⑥为Cl、⑦为Ar、⑧为K、⑨为Ca、⑩为Se.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强;
(2)元素非金属性越强,其氢化物越稳定;
(3)稀有气体Ar原子核外最外层为稳定结构,化学性质最不活泼,Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(4)上述元素的最高价氧化物的水化物中酸性最强是高氯酸;
(5)电子层结构相同,核电荷数越大离子半径越小;
(6)⑨和⑩均处于第四周期,⑨位于第2列,⑩位于第16列,第四周期中每列容纳1种元素,故二者原子序数之差等于所在列数之差;
(7)Se与S同主族,可知Se的常见化合价为+4、+6,据此书写其氧化物化学式.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强;
(2)元素非金属性越强,其氢化物越稳定;
(3)稀有气体Ar原子核外最外层为稳定结构,化学性质最不活泼,Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(4)上述元素的最高价氧化物的水化物中酸性最强是高氯酸;
(5)电子层结构相同,核电荷数越大离子半径越小;
(6)⑨和⑩均处于第四周期,⑨位于第2列,⑩位于第16列,第四周期中每列容纳1种元素,故二者原子序数之差等于所在列数之差;
(7)Se与S同主族,可知Se的常见化合价为+4、+6,据此书写其氧化物化学式.
解答:
解:由元素在周期表中位置,可知①为C、②为O、③为Al、④为Si、⑤为S、⑥为Cl、⑦为Ar、⑧为K、⑨为Ca、⑩为Se.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,故上述元素中K元素金属性最强,故答案为:K;
(2)Al与H形成金属氢化物,不是气体,同周期自左而右非金属性增强,同主族自上而下非金属性减弱,元素①~⑥中Si的非金属性最弱,其氢化物SiH4最不稳定,故答案为:SiH4;
(3)稀有气体Ar原子核外最外层为稳定结构,化学性质最不活泼,Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8,其原子结构示意图为: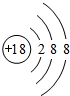 ,故答案为:
,故答案为: ;
;
(4)上述元素的最高价氧化物的水化物中酸性最强是高氯酸,其化学式为HClO4,故答案为:HClO4;
(5)电子层结构相同,核电荷数越大离子半径越小,故离子半径:S2->Cl->K+>Ca2+,故答案为:S2-;
(6)⑨和⑩均处于第四周期,⑨位于第2列,⑩位于第16列,第四周期中每列容纳1种元素,故二者原子序数之差等于所在列数之差,即二者原子序数相差16-2=14,故答案为:14;
(7)Se与S同主族,可知Se的常见化合价为+4、+6,对应氧化物化的化学式分别为:SeO2、SeO3,故答案为:SeO2;SeO3.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,故上述元素中K元素金属性最强,故答案为:K;
(2)Al与H形成金属氢化物,不是气体,同周期自左而右非金属性增强,同主族自上而下非金属性减弱,元素①~⑥中Si的非金属性最弱,其氢化物SiH4最不稳定,故答案为:SiH4;
(3)稀有气体Ar原子核外最外层为稳定结构,化学性质最不活泼,Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8,其原子结构示意图为:
 ,故答案为:
,故答案为: ;
;(4)上述元素的最高价氧化物的水化物中酸性最强是高氯酸,其化学式为HClO4,故答案为:HClO4;
(5)电子层结构相同,核电荷数越大离子半径越小,故离子半径:S2->Cl->K+>Ca2+,故答案为:S2-;
(6)⑨和⑩均处于第四周期,⑨位于第2列,⑩位于第16列,第四周期中每列容纳1种元素,故二者原子序数之差等于所在列数之差,即二者原子序数相差16-2=14,故答案为:14;
(7)Se与S同主族,可知Se的常见化合价为+4、+6,对应氧化物化的化学式分别为:SeO2、SeO3,故答案为:SeO2;SeO3.
点评:本题考查元素周期表与元素周期律,难度不大,侧重对元素周期律的考查,注意把握元素周期表的结构,掌握金属性、非金属性强弱比较.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
C7H16的同分异构体中,同时含有3个甲基的结构有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
在水溶液中,YO3-与S2-发生反应的离子方程式:YO3-+3S2-+6H+═Y-+3S+3H2O,下列有关叙述或推导正确的是( )
| A、YO3-体现了还原性 |
| B、若Y为短周期元素,则Y对应的元素有2种可能 |
| C、Y可能位于ⅤA 族 |
| D、Y最外层有7个电子 |
在理论上不能用于设计原电池的化学反应是( )
| A、2FeCl3(aq)+2KI(aq)═2FeCl2(aq)+2KCl(aq)+I2(aq)△H<0 |
| B、Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3?H2O(aq)+8H2O(l)△H>0 |
| C、4Al(s)+6H2O(l)+3O2(g)═4Al(OH)3(s)△H<0 |
| D、Zn(s)+2MnO2(s)+2H2O(l)═2MnOOH(s)+Zn(OH)2(s)△H<0 |
下列有机物中,含有两种官能团的是( )
| A、CH2=CH-CH2Cl |
B、 |
| C、CH3CHO |
| D、CH3CH2OH |
