题目内容
室温下,已知某溶液中由水电离的c(H+)和c(OH-)浓度的乘积为10-20,则该溶液中,一定不能大量共存的离子是( )
| A、S2- |
| B、NH4+ |
| C、CO32- |
| D、HCO3- |
考点:水的电离,离子共存问题
专题:离子反应专题
分析:根据由水电离出的c(H+)和c(OH-)浓度的乘积为10-20,可知水电离的c(H+)=10-10,则水的电离收到抑制,说明溶液为碱或者酸,根据离子是否与酸碱反应来判断.
解答:
解:根据由水电离出的c(H+)和c(OH-)浓度的乘积为10-20,可知水电离的c(H+)=10-10,溶液为碱或者酸.
A、S2-与氢离子反应,与氢氧根离子不反应,若为碱,则能大量共存,故A不选;
B、NH4+和氢氧根离子反应,与氢离子离子不反应,可共存于酸性溶液,故B不选;
C、CO32-和氢离子反应,与氢氧根离子不反应,可共存于碱性溶液,故C不选;
D、HCO3-和氢氧根离子、氢离子都反应,一定不能大量共存,故D选;
故选D.
A、S2-与氢离子反应,与氢氧根离子不反应,若为碱,则能大量共存,故A不选;
B、NH4+和氢氧根离子反应,与氢离子离子不反应,可共存于酸性溶液,故B不选;
C、CO32-和氢离子反应,与氢氧根离子不反应,可共存于碱性溶液,故C不选;
D、HCO3-和氢氧根离子、氢离子都反应,一定不能大量共存,故D选;
故选D.
点评:本题考查了离子共存的判断,根据水电离出的c(H+)和c(OH-)浓度的乘积为10-20,算出水电离的氢离子浓度,溶液可能显示酸性、碱性,本题难度不大.

练习册系列答案
相关题目
下列事实不能用勒夏特列原理(平衡移动原理)解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
| A、①②③ | B、②④⑥ |
| C、③④⑤ | D、②⑤⑥ |
有一分子式为C8H14N2O3的二肽,经水解后得到丙氨酸CH3CH(NH2)COOH和另一种氨基酸R,则R的分子式为( )
| A、C5H9NO |
| B、C5H9NO2 |
| C、C5H9NO3 |
| D、C5H9NO4 |
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O═7X+5FeSO4+12H2SO4,下列说法正确的是( )
| A、X的化学式为CuS,它既是氧化产物又是还原产物 |
| B、5 mol FeS2发生反应,有10 mol电子转移 |
| C、产物中的SO42-离子有一部分是氧化产物 |
| D、FeS2只作还原剂 |
下列物质都能导电,其中属于电解质的是( )
| A、NaCl溶液 | B、铝丝 |
| C、盐酸 | D、熔融的NaOH |
人们利用纳米级(1~100nm,1nm=10-9m)粒子物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用.将纳米级粒子物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述不正确的是( )
| A、该分散系能产生丁达尔效应 |
| B、该分散质颗粒能透过滤纸 |
| C、该分散质颗粒能透过半透膜 |
| D、该分散质颗粒能发生布朗运动 |
按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物.下列生产乙醇的反应中,原子利用率最高的是( )
A、乙烯水化:CH2=CH2+H2O
| |||
B、葡萄糖发酵:C6H12O6
| |||
C、溴乙烷水解:CH3CH2Br+H2O
| |||
D、丙酸乙酯水解:CH3CH2COOCH2CH3+H2O
|
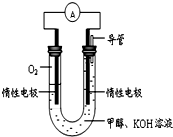 某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.