题目内容
20.含铬(Cr)工业废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀.转化过程中,废水pH与Cr2O72-转化为Cr3+的关系如图1所示,实验室模拟工业电解法处理含铬废水的装置如图2所示.
请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是调节pH为1左右.
(2)写出下列反应的离子方程式:
①电解过程中的阴极反应式2H++2e-═H2↑;
②Cr2O72-转化为Cr3+的离子方程式6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
分析 (1)根据废水pH与Cr2O72-转化为Cr3+的关系图1分析;
(2)①阴极,根据放电顺序阴极上是电解质中氢离子得电子的反应;
②在电解池中,阳极是活泼金属铁电极时,则电极本身失去电子,即Fe-2e-=Fe2+,重铬酸根具有强氧化性,能将生成的亚铁离子氧化为三价,据此书写离子方程式;
解答 解:(1)根据废水pH与Cr2O72-转化为Cr3+的关系图1可知:当pH为1时,Cr2O72-转化为Cr3+的转化率接近100%,
故答案为:调节pH为1左右;
(2)①阴极,根据放电顺序阴极上是电解质中氢离子得电子的反应,即2H++2e=H2↑,故答案为:2H++2e-═H2↑;
②在电解池中,阳极是活泼金属铁电极时,则电极本身失去电子,即Fe-2e-=Fe2+,重铬酸根具有强氧化性,能将生成的亚铁离子氧化为三价,即6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
点评 本题考查氧化还原反应、电解原理等,需要学生具备扎实的基础知识,平时注意培养分析和解决问题的能力,题目难度中等.

练习册系列答案
相关题目
8.多数晶体中的微观微粒服从紧密堆积原理的根本原因是( )
| A. | 便于形成规则的几何外形 | |
| B. | 微观微粒结合得越紧密,体系总能量越低,体系越稳定 | |
| C. | 便于使晶体具有对称性 | |
| D. | 为了使晶体具备各向异性 |
9.下列叙述错误的是( )
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 1H和2H是不同的核素,它们的质子数相等 | |
| C. | ${\;}_{90}^{230}$Th与${\;}_{90}^{232}$Th互为同素异形体 | |
| D. | ${\;}_{1}^{1}$ H、${\;}_{1}^{2}$ H、${\;}_{1}^{3}$ H、H+、H2是氢元素的五种不同粒子 |
8.关于1L 0.1mol/L 的(NH4)2Fe(SO4)2溶液,下列说法正确的是( )
| A. | Cl-、I-、Na+能在该溶液中大量共存 | |
| B. | 通入H2S气体,发生反应的离子方程式为:H2S+Fe2+═FeS↓+2H+ | |
| C. | Ca2+、ClO-、Cl-、Cu2+能在该溶液中大量共存 | |
| D. | 和少量的NaOH溶液充分反应并加热,可生成标准状况下的NH3 4.48L |
5.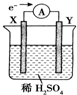 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 溶液中,SO42-朝Y极移动 | |
| B. | 若两电极分别为铁和碳棒,则X为碳棒,Y为铁 | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 若两电极都是金属,则它们的活动性顺序为X>Y |
12.下列叙述中正确的是( )


| A. | 图①中正极附近溶液pH减小 | |
| B. | 图①中电子由Zn流向Cu,盐桥中的Cl-移向CuSO4溶液 | |
| C. | 图②正极反应是O2+2H2O+4e-═4OH- | |
| D. | 图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
9. 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO
d.NaHCO3; pH由小到大的排列顺序是(填序号)a<d<c<b.
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,
下列表达式的数据变大的是BD.
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)•c(OH-)
D.c(OH-)/c(H+) E.c(H+)•c(CH3COO-)/c(CH3COOH)
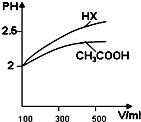
(3)体积均为100ml pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX)> Ka(CH3COOH)(填>、<或=).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中自由离子浓度的从大到小
的关系为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO
d.NaHCO3; pH由小到大的排列顺序是(填序号)a<d<c<b.
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,
下列表达式的数据变大的是BD.
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)•c(OH-)
D.c(OH-)/c(H+) E.c(H+)•c(CH3COO-)/c(CH3COOH)
(3)体积均为100ml pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX)> Ka(CH3COOH)(填>、<或=).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中自由离子浓度的从大到小
的关系为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
10.下列物质中,既能与盐酸反应,又能与KOH溶液反应的是( )
①NaHCO3
②AgNO3③(NH4)2S
④HOOC-COONa
⑤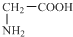
⑥
①NaHCO3
②AgNO3③(NH4)2S
④HOOC-COONa
⑤
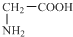
⑥

| A. | 全部 | B. | ①②④⑤⑥ | C. | ②③④⑤⑥ | D. | ②④⑤⑥ |
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL 1mol•L-1的稀硫酸.
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL 1mol•L-1的稀硫酸.