题目内容
已知下列三个热化学方程式
①H2(g)+
O2(g)═H2O(g)△H=-241.8kJ?mol-1
②C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
③C(s)+H2O(g)═CO(g)+H2(g)△H=+131kJ?mol-1
写出表示碳燃烧生成CO和CO燃烧生成CO2的燃烧热的热化学方程式. ; .
①H2(g)+
| 1 |
| 2 |
②C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
③C(s)+H2O(g)═CO(g)+H2(g)△H=+131kJ?mol-1
写出表示碳燃烧生成CO和CO燃烧生成CO2的燃烧热的热化学方程式.
考点:热化学方程式
专题:化学反应中的能量变化
分析:依据热化学方程式和盖斯定律分析计算,利用热化学方程式加减得到所需热化学方程式,燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,碳燃烧生成一氧化碳放出的热量利用①③计算,一氧化碳燃烧生成二氧化碳的燃烧热利用②-碳燃烧生成一氧化碳的热化学方程式得到.
解答:
解:依据盖斯定律①+③得到碳燃烧生成一氧化碳反应的热化学方程式为:③C(s)+
O2(g)═CO(g)△H=-110.8 kJ?mol-1 ;
依据盖斯定律②-③得到,CO燃烧生成CO2的燃烧热的热化学方程式,CO (g)+
O2(g)═CO2(g)△H=-282.7 kJ?mol-1;
故答案为:C(s)+
O2(g)═CO(g)△H=-110.8 kJ?mol-1 ;CO (g)+
O2(g)═CO2(g)△H=-282.7 kJ?mol-1;
| 1 |
| 2 |
依据盖斯定律②-③得到,CO燃烧生成CO2的燃烧热的热化学方程式,CO (g)+
| 1 |
| 2 |
故答案为:C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
点评:本题考查了热化学方程式和盖斯定律的计算应用,注意燃烧热概念的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
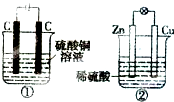 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A、产生气体体积:①=② |
| B、溶液的pH变化:①减小,②增大 |
| C、电极反应式:①中阳极为4 OH--4e-=2H2O+O2↑②中负极为2H++2e-=H2↑ |
| D、①中阴极质量增加,②中正极质量减小 |
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
| B、等物质的量浓度、等体积的Na2S与KHSO3溶液混合c (Na+)>c(K+)>c(SO32-)>c(HS-)>c(OH-)>c((H+) |
| C、在0.1mol?L-1NaHSO3溶液中有c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3) |
| D、pH<7的某二元弱酸的酸式盐NaHA溶液中有c(H+)+2c(A2-)═c(OH-)+c(H2A) |
中学化学教材中,常借助于图象的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理.下列有关化学图象表现的内容正确的是( )
A、 除去Cl2中的HCl杂质 |
B、 稀释浓硫酸 |
C、 检查装置气密性 |
D、 实验室制取NH3 |




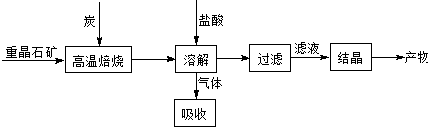
 如图两个装置中用滴有酚酞的NaCl溶液做电解质溶液,进行化学能和电能相互转化的研究.请回答:
如图两个装置中用滴有酚酞的NaCl溶液做电解质溶液,进行化学能和电能相互转化的研究.请回答: