题目内容
现有A,B,C,D四种元素,A,B两种元素的原子各有两个电子层,C,D两种元素的原子各有三个电子层.A和B能化合成无色无味的气体AB2,C和D能形成化合物CD,D和B的原子的最外电子层上电子数相同,B的简单离子和C的简单离子的核外电子数相等.
(1)写出A,B,C三种元素的名称:A为 ,B为 ,C为 ;
(2)D元素原子结构示意图是 ;
(3)D元素与钠元素形成的化合物的电子式是 .
(1)写出A,B,C三种元素的名称:A为
(2)D元素原子结构示意图是
(3)D元素与钠元素形成的化合物的电子式是
考点:原子核外电子排布
专题:原子组成与结构专题
分析:现有A、B、C、D四种元素,A、B两种元素的原子各有两个电子层,C、D两种元素的原子各有三个电子层.A和B能化合成无色无味的气体AB2,可推知A为C元素、B为O元素,D和B的原子的最外电子层上电子数相同,则D为S元素,C和D能形成化合物CD,C表现+2价,B的简单离子和C的简单离子的核外电子数相等,则C为Mg,据此解答.
解答:
解:现有A、B、C、D四种元素,A、B两种元素的原子各有两个电子层,C、D两种元素的原子各有三个电子层.A和B能化合成无色无味的气体AB2,可推知A为C元素、B为O元素,D和B的原子的最外电子层上电子数相同,则D为S元素,C和D能形成化合物CD,C表现+2价,B的简单离子和C的简单离子的核外电子数相等,则C为Mg,
(1)由上述分析可知,A为碳,B为氧,C为镁,故答案为:碳;氧;镁;
(2)D为S元素,其原子结构示意图是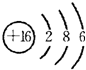 ,故答案为:
,故答案为: ;
;
(3)S元素与钠元素形成的化合物为Na2S,属于离子化合物,其电子式是 ,故答案为:
,故答案为: .
.
(1)由上述分析可知,A为碳,B为氧,C为镁,故答案为:碳;氧;镁;
(2)D为S元素,其原子结构示意图是
 ,故答案为:
,故答案为: ;
;(3)S元素与钠元素形成的化合物为Na2S,属于离子化合物,其电子式是
 ,故答案为:
,故答案为: .
.
点评:本题考查核外电子排布、电子式等,比较基础,推断元素是解题关键,元素所在周期及A和B能化合成无色无味的气体AB2是推断突破口,难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
下列有关有机物的叙述正确的是( )
| A、苯与乙烯均能与溴水发生加成反应,而甲烷只能与溴水发生取代反应 |
| B、煤井中的瓦斯气和家庭使用的液化石油气的主要成分都是甲烷 |
C、苯的结构简式为 ,分子式可简化为CH ,分子式可简化为CH |
| D、利用酸性KMnO4溶液可鉴别乙烯和乙烷 |
A、B、C为三中短周期元素,A、B在同一周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构.下列说法中正确的是( )
| A、原子半径:A>B>C |
| B、离子半径 A2->B2+>C- |
| C、离子半径 A2->C->B2+ |
| D、原子最外层电子数:A>C>B |