题目内容
10.下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是( )| A. | 将甲、乙作电极组成原电池时,甲是负极 | |
| B. | 同价态的阳离子,甲比乙的氧化性强 | |
| C. | 甲与稀盐酸反应放出氢气的体积比乙与稀盐酸反应放出氢气的体积大 | |
| D. | 在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 |
分析 A.原电池的负极金属活泼性强于正极金属;
B.金属元素的金属性越强,其阳离子的氧化性越弱;
C.金属性越强,和与酸反应置换氢的难易程度有关;
D.金属元素的金属性强弱与得失电子的难易程度有关.
解答 解:A.两种金属单质作电极组成的原电池,活动性较强的作负极,较弱的作正极,将甲、乙作电极组成原电池时,甲是负极,则金属甲的活动性比金属乙的活动性强,故A正确;
B.金属的还原性越强,其对应的阳离子的氧化性越弱,同价态的阳离子,甲比乙的氧化性强,则甲的金属性比乙弱,故B错误;
C.金属与盐酸反应,活动性越强反应速率越快,与生成氢气的体积无必然联系,故C错误;
D.还原性越强,失电子能力越强,与失去电子数目无关,故D错误.
故选A.
点评 本题考查了金属活泼性的判断方法,要注意的是:金属的金属性强弱与得失电子的难易有关,与得失电子的多少无关,题目难度不大.

练习册系列答案
相关题目
20.表是元素周期表的一部分,请用元素符号或者相关化学式回答有关问题:
(1)表中能形成两性氢氧化物的元素在周期表中的位置是第三周期第ⅢA;
(2)写出②的气态氢化物的结构式 ;
;
(3)元素④⑤⑥⑦离子半径由大到小的顺序S2->Cl->Mg2+>Al3+;
(4)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是HClO4;
(5)⑥和⑦阴离子还原性较强的是S2-用一个置换反应证实这一结论(写化学方程式)Cl2+S2-=S+2Cl-;
(6)④⑤两元素相比较,金属性较强的是Mg,可以验证该结论的实验是bc;
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质用砂纸打磨后分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质用砂纸打磨后分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
(7)设计实验比较⑦⑩的非金属性强弱(实验药品:KBr溶液、KCl溶液、氯水、溴水,简述实验操作及现象向KBr溶液中滴加氯水,溶液变黄色,写出相关的离子方程式Cl2+2Br-=Br2+2Cl-.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)写出②的气态氢化物的结构式
 ;
;(3)元素④⑤⑥⑦离子半径由大到小的顺序S2->Cl->Mg2+>Al3+;
(4)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是HClO4;
(5)⑥和⑦阴离子还原性较强的是S2-用一个置换反应证实这一结论(写化学方程式)Cl2+S2-=S+2Cl-;
(6)④⑤两元素相比较,金属性较强的是Mg,可以验证该结论的实验是bc;
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质用砂纸打磨后分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质用砂纸打磨后分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
(7)设计实验比较⑦⑩的非金属性强弱(实验药品:KBr溶液、KCl溶液、氯水、溴水,简述实验操作及现象向KBr溶液中滴加氯水,溶液变黄色,写出相关的离子方程式Cl2+2Br-=Br2+2Cl-.
18.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)③元素与⑩元素两者核电荷数之差是26.
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下列空格.
实验原理(化学方程式):Cl2+2NaBr=2NaCl+Br2
实验步骤:将少量氯水加入盛有溴化钠溶液的试管中,振荡后,加入少量四氯化碳,振荡
实验现象:若加入氯水后溶液呈黄色,加入少量四氯化碳后,四氯化碳层呈棕色;
结论:证明单质氯比单质溴氧化性强..
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)③元素与⑩元素两者核电荷数之差是26.
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下列空格.
实验原理(化学方程式):Cl2+2NaBr=2NaCl+Br2
实验步骤:将少量氯水加入盛有溴化钠溶液的试管中,振荡后,加入少量四氯化碳,振荡
实验现象:若加入氯水后溶液呈黄色,加入少量四氯化碳后,四氯化碳层呈棕色;
结论:证明单质氯比单质溴氧化性强..
5.下表是元素周期表的一部分,针对表中元素,填写下列空白.
(1)写出Na+结构示意图 ,氯元素的原子结构示意图
,氯元素的原子结构示意图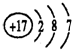 ;
;
(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 ,氯元素的原子结构示意图
,氯元素的原子结构示意图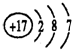 ;
;(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式
 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
15.有关下列物质的应用说法正确的是( )
| A. | 纯碱常用于治疗胃酸过多 | |
| B. | 硫酸亚铁可用作缺铁性贫血的补血剂 | |
| C. | 用明矾进行自来水的杀菌消毒 | |
| D. | 碳酸钙不能用作人体补钙剂 |
2.最近媒体报道了一些化学物质,如爆炸力极强的N5,结构类似白磷的P4,比黄金还贵的18O2,太空中的甲醇气团等.下列说法正确的是( )
| A. | 2N5═5N2是化学变化 | B. | 18O2和16O2是同位素 | ||
| C. | 18O的原子内有9个中子 | D. | P4只有共价键 |
19.下列说法不正确的是( )
| A. | 微粒半径:Cl>S>N>O | B. | 稳定性:HF>HCl>HBr>HI | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |
20.下列反应过程中的能量变化情况符合如图的是( )
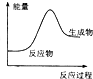

| A. | 氧化钙溶于水 | B. | 碳酸钙高温煅烧分解 | ||
| C. | 酸和碱的中和反应 | D. | 铝粉与氧铁粉末反应 |
 .
.