题目内容
13.对于化学反应方向的确定不仅与焓变(△H)有关,也与温度(T)、熵变(△S)有关,实验证明,化学反应的方向应由△H-T△S确定,若△H-T△S<0则自发进行,否则不能自发进行,下列说法中,正确的是( )| A. | 在温度、压力一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 | |
| B. | 温度、压力一定时,放热的熵增加反应不一定能自发进行 | |
| C. | 反应焓变是决定反应能否自发进行的唯一因素 | |
| D. | 固体的溶解过程只与焓变有关 |
分析 A、反应自发进行的判断依据是△H-T△S<0,则能自发进行;
B、应自发进行的判断依据是△H-T△S<0,则能自发进行;
C、反应自发进行由焓变、熵变、温度共同决定;
D、固体溶解主要是物理过程,焓变是反应前后的能量变化.
解答 解:A、在温度、压力一定的条件下,焓因素和熵因素共同决定一个化学反应的方向,△H-T△S<0,则能自发进行;△H-T△S>0,则不能自发进行;故A正确;
B、温度、压力一定时,放热的熵增加反应,△H<0,△S>0,△H-T△S<0,反应一定能自发进行,故B错误;
C、反应自发进行由焓变、熵变、温度共同决定,故C错误;
D、固体溶解主要是物理过程,焓变是反应前后的能量变化;故D错误;
故选A.
点评 本题考查了反应自发进行的判断依据,物质变化过程焓变熵变的变化是解题关键,题目较简单.

练习册系列答案
相关题目
3.下列实验叙述正确的是( )
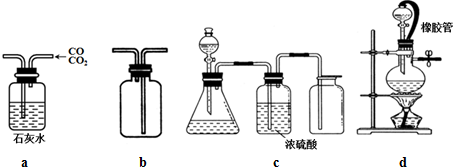

| A. | 用a装置除去混合气体中的杂质CO2 | |
| B. | 用b装置排气法收集H2、NH3、Cl2 | |
| C. | c装置用于碳酸钙和浓盐酸反应制取纯净CO2 | |
| D. | d中橡胶管可使烧瓶内的压强与大气压保持一致,便于液体滴下 |
4.如图装置能达到实验目的是( )
| A. | 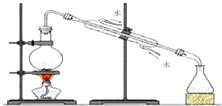 制取少量纯净的水 | B. |  除去Cl2中HCl杂质 | ||
| C. |  烧瓶内形成蓝色喷泉 | D. | 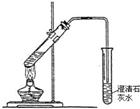 探究NaHCO3的热稳定性 |
1.下列表示对应化学反应的离子方程式正确的是( )
| A. | NaHS溶液中通入Cl2:S2-+Cl2═S↓+2Cl- | |
| B. | NaN02溶液中滴加酸性KMnO4溶液:5NO2-+2MnO4-+3H2O═5NO3-+2Mn2++6OH- | |
| C. | NH4HSO4溶液中滴加少量的Ba(OH)2溶液:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| D. | 硫酸亚铁酸性溶液中加入过氧化氢:2Fe2++H2O2+2H+═2Fe3++2H2O |
8.反应:2H2(g)+O2(g)═2H2O(l)过程中的能量变化如图所示,下列有关说法中正确的是( )
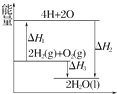

| A. | △H<0 | B. | △H2为该反应的反应热 | ||
| C. | △H3不是H2的燃烧热 | D. | △H3=△H1+△H3 |
18.下列说法正确的是( )
| A. | SO2和CO都是酸性氧化物,都能与水反应 | |
| B. | Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 | |
| C. | Al2O3和Na2O按物质的量比1:1投入水中可得到澄清溶液 | |
| D. | 金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气 |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,Na2O2与足量的CO2反应生成2.24LO2,转移电子数为0.4NA |
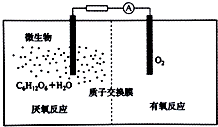 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.