题目内容
已知:C(s)+H2O(I)=CO(g)+H2(g)△H1═+175.3kJ/mol
CO(g)+
O2(g)═CO2(g)△H2═-283.0kJ/mol
H2(g)+
O2(g)═H2O(Ⅰ)△H3═-283.0kJ/mol
则C(s)+O2(g)═CO2(g)的△H等于( )
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
则C(s)+O2(g)═CO2(g)的△H等于( )
| A、390.7kj/mol |
| B、-679.3kj/mol |
| C、-787kj/mol |
| D、+180.9kj/mol |
考点:有关反应热的计算,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:依据题干热化学方程式,结合盖斯定律的内容是与起始状态和终了状态有关,与变化过程无关,进行计算.
解答:
解:①C(s)+H2O(l)=CO(g)+H2(g)△H1═+175.3kJ/mol
②CO(g)+
O2(g)═CO2(g)△H2═-283.0kJ/mol
③H2(g)+
O2(g)═H2O(l)△H3═-283.0kJ/mol
依据盖斯定律①+②+③得到C(s)+O2(g)═CO2(g)△H,由此可知△H=△H1+△H2+△H3═-390.7kJ/mol
故选A
②CO(g)+
| 1 |
| 2 |
③H2(g)+
| 1 |
| 2 |
依据盖斯定律①+②+③得到C(s)+O2(g)═CO2(g)△H,由此可知△H=△H1+△H2+△H3═-390.7kJ/mol
故选A
点评:本题考查了盖斯定律的计算应用,注意热化学方程式系数变化焓变随之变化,反应改变方向,焓变改变符号,题目较简单.

练习册系列答案
相关题目
把100mL 2mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的( )
| A、硫酸铜溶液 |
| B、硝酸钠溶液 |
| C、醋酸钠溶液 |
| D、氢氧化钠溶液 |
下列判断不正确的是( )
| A、沸点:NH3>PH3>AsH3 |
| B、熔点:Si3N4>NaCl>SiI4 |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
下列有关说法不正确的是( )
| A、高容量储氢材料的研制是推广应用氢氧燃料电池的关键问题之一 |
| B、发展低碳经济,推广可利用太阳能的城市照明系统有利于节能减排、改善环境质量 |
| C、仅需要托盘天平、砝码、药匙、一定规格的容量瓶、烧杯、玻璃棒这些仪器就可以准确配制出一定浓度的NaCL溶液 |
| D、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
关于1mol H2O的叙述正确的是( )
| A、含有1mol氢气 |
| B、质量为18g/mol |
| C、在标准状况下的体积为22.4L |
| D、含有水分子的个数约为6.02×1023 |
下列化学方程式不正确的是( )
A、乙醇与浓氢溴酸反应CH3CH2OH+HBr
| |||
B、溴乙烷与氢氧化钠溶液共热CH3CH2Br+NaOH
| |||
C、苯酚钠中通入二氧化碳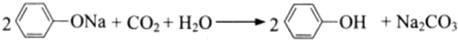 | |||
D、蔗糖在稀硫酸作用下水解C12H22011(蔗糖)+H2O
|
下列选项中正确的是( )
| A、1L 0.5mol?L-1稀硫酸与1L 1mol?L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l);△H=-57.3kJ?mol-1 | ||||
| B、某酸的酸式盐NaHY水溶液显碱性,则H2Y?2H++Y2- | ||||
| C、纯碱溶液显碱性的原因用离子方程式可表示为:CO32-+2H2O?H2CO3+2OH- | ||||
D、以惰性电极电解KCl溶液的离子方程式为:2Cl-+2H2O
|
 如图为某市售盐酸试剂瓶标签上的部分数据.问:
如图为某市售盐酸试剂瓶标签上的部分数据.问: