题目内容
14.低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为2NH3(g)+NO(g)+NO2(g)$→_{催化剂}^{150℃}$2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法不正确的是( )| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数减小 | |
| B. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率增大 | |
| C. | 单位时间内消耗NO和N2的物质的量比为1:1时,反应达到平衡 | |
| D. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率不变 |
分析 A.从平衡移动的方向判断平衡常数的变化;
B.可逆反应中,加入一种反应物,平衡向正方向移动,以此判断转化率变化;
C.反应达到平衡时,正逆反应速率相等;
D.催化剂能加快反应速率,但不影响平衡的移动.
解答 解:A.反应为放热反应,升高温度可使反应逆向移动,生成物浓度减小,反应物浓度增大,故K值减小,故A正确;
B.增加NH3的浓度,可使反应正向移动,NO、NO2转化率增大,故B正确;
C.平衡时,NO和N2消耗的物质的量之比为1:2,故C错误;
D.使用催化剂可加快反应速率,但不改变平衡,故D正确;
故选C.
点评 本题考查外界条件对化学反应速率的影响、平衡状态的判断等问题,题目难度中等,做题时注意平衡常数的变化以及平衡状态的判断方法等问题,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
4.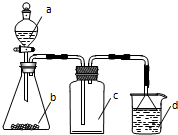 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )
 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )| 选项 | a中物质 | b中物质 | c中的气体 | d中物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 稀硝酸 | Cu | NO | H2O |
| C | 硫酸 | Na2CO3 | CO2 | NaOH溶液 |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.某无色强酸溶液中,能大量共存的离子组是( )
| A. | NH4+、NO3-、Al3+、K+ | B. | Na+、NO3-、S2-、K+ | ||
| C. | MnO4-、SO32-、Na+、K+ | D. | HCO3-、SO42-、Na+、K+ |
2.X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如表所示.已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素.下列说法错误的是( )
| X | ||||
| Z | W |
| A. | X和氢组成的化合物分子中可能含有极性共价键和非极性共价键 | |
| B. | 工业上用电解Y和W组成的化合物来制备Y | |
| C. | Z、W两元素的气态氢化物中,W的气态氢化物更稳定 | |
| D. | X、Y、Z、W元素最高价氧化物对应的水化物中酸性最强的是HWO4 |
19.X、Y、Z、R、W是五种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
| A. | 离子半径:Y2->Z+ | |
| B. | 气态氢化物稳定性:HW>H2R | |
| C. | XW4分子中各原子均满足8电子稳定结构 | |
| D. | Y、Z、R三种元素组成的化合物只含有离子键 |
6.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O2 ? CO2 | ||
| C. | CaCl2 NaOH H2O | D. | CH4 H2O CS2 |
3.关于反应N2+3H2$?_{△}^{催化剂}$2NH3的说法错误的是( )
| A. | 外界条件可以改变平衡状态 | B. | 达到平衡时正、逆反应速率相等 | ||
| C. | 平衡时各组分的含量也在不断变化 | D. | 该反应所建立的平衡是动态平衡 |
4.下列对分子及其性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子而HClO为0 |