题目内容
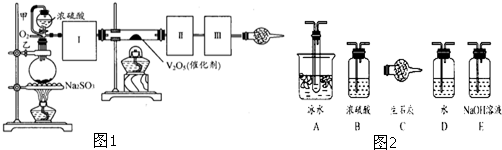
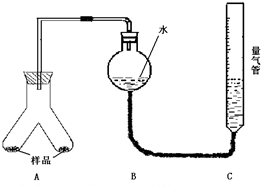
用如图1装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是16.8℃,沸点是44.8℃.
(1)写出圆底烧瓶中所发生的化学方程式
(2)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图2A~E装置中选择最适合装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 、 、 .
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是 .
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(任写一条).原因 ,验证方法
(5)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5NA个电子转移时,该反应的化学方程式
(6)用amol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)

(1)写出圆底烧瓶中所发生的化学方程式
(2)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图2A~E装置中选择最适合装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(任写一条).原因
(5)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5NA个电子转移时,该反应的化学方程式
(6)用amol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)圆底烧瓶中所发生的化学方程式为Na2SO3+H2SO4(浓)
Na2SO4+SO2↑+H2O;
(2)二氧化硫的干燥用浓硫酸,当温度低于16.8℃可以获得三氧化硫的晶体,尾气处理用烧碱溶液;
(3)为保证生成的二氧化硫尽可能的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作;
(4)亚硫酸钠变质会生成硫酸钠,根据检验亚硫酸钠中硫酸根是否存在来证明结论;亚硫酸钠和稀硫酸反应产生的二氧化硫速率很慢;
(5)SO2通入含1.0mol次氯酸的溶液中,根据转移的电子数来确定两种强酸;
(6)根据S元素守恒计算消耗的物质的量,可计算转化率.
| ||
(2)二氧化硫的干燥用浓硫酸,当温度低于16.8℃可以获得三氧化硫的晶体,尾气处理用烧碱溶液;
(3)为保证生成的二氧化硫尽可能的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作;
(4)亚硫酸钠变质会生成硫酸钠,根据检验亚硫酸钠中硫酸根是否存在来证明结论;亚硫酸钠和稀硫酸反应产生的二氧化硫速率很慢;
(5)SO2通入含1.0mol次氯酸的溶液中,根据转移的电子数来确定两种强酸;
(6)根据S元素守恒计算消耗的物质的量,可计算转化率.
解答:
解:(1)圆底烧瓶中所发生的化学方程式为Na2SO3+H2SO4(浓)
Na2SO4+SO2↑+H2O;故答案为:Na2SO3+H2SO4(浓)
Na2SO4+SO2↑+H2O;
(2)SO2转化成SO3之前必须对二氧化硫进行干燥,可以用浓硫酸,SO3的熔点是16.8℃,沸点是44.8℃,当温度低于 16.8℃时,三氧化硫以晶体状态存在,二氧化硫、三氧化硫的尾气处理用烧碱溶液吸收,故答案为:B;A;E;
(3)为保证生成的二氧化硫尽可能多的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作,保证生成的二氧化硫尽可能的参与反应,故答案为:先加热催化剂再滴入浓硫酸;
(4)影像化学反应速率的因素有:浓度、温度等,亚硫酸钠变质会生成硫酸钠,硫酸钠和浓硫酸不反应;此外亚硫酸钠和稀硫酸反应产生的二氧化硫速率会很慢,可能的原因是Na2SO3变质,可通过取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;故答案为:Na2SO3变质;取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;
(5)SO2通入含1.0mol次氯酸的溶液中,转移的电子为2mol,所以是1molSO2和1mol次氯酸反应生成盐酸和硫酸,
故答案为:SO2+H2O+HClO═HCl+H2SO4;
(6)根据元素守恒Na2SO3~SO2,则amol会生成二氧化硫amol,装置Ⅲ增重了bg,说明剩余的二氧化硫为bg
(即
=
mol),所以二氧化硫的转化率=
×100%=
%,
故答案为:
.
| ||
| ||
(2)SO2转化成SO3之前必须对二氧化硫进行干燥,可以用浓硫酸,SO3的熔点是16.8℃,沸点是44.8℃,当温度低于 16.8℃时,三氧化硫以晶体状态存在,二氧化硫、三氧化硫的尾气处理用烧碱溶液吸收,故答案为:B;A;E;
(3)为保证生成的二氧化硫尽可能多的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作,保证生成的二氧化硫尽可能的参与反应,故答案为:先加热催化剂再滴入浓硫酸;
(4)影像化学反应速率的因素有:浓度、温度等,亚硫酸钠变质会生成硫酸钠,硫酸钠和浓硫酸不反应;此外亚硫酸钠和稀硫酸反应产生的二氧化硫速率会很慢,可能的原因是Na2SO3变质,可通过取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;故答案为:Na2SO3变质;取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;
(5)SO2通入含1.0mol次氯酸的溶液中,转移的电子为2mol,所以是1molSO2和1mol次氯酸反应生成盐酸和硫酸,
故答案为:SO2+H2O+HClO═HCl+H2SO4;
(6)根据元素守恒Na2SO3~SO2,则amol会生成二氧化硫amol,装置Ⅲ增重了bg,说明剩余的二氧化硫为bg
(即
| bg |
| 64g/mol |
| b |
| 64 |
a-
| ||
| a |
| 1600a-25b |
| 16a |
故答案为:
| 1600a-25b |
| 16a |
点评:本题主要考查了二氧化硫的性质以及离子的检验等知识,综合性较强,难度较大,考查学生分析和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列电离方程式的书写正确的是( )
| A、CuCl2=Cu+Cl2↑ |
| B、Na2CO3=2Na++CO32- |
| C、H2SO4=2H++S6++4O2- |
| D、NaHCO3=Na++H++CO32- |
下列有关问题,与盐类的水解无关的是( )
| A、NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| B、盐酸可作铁制品的除锈剂 |
| C、实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 |
| D、加热蒸干AlCl3溶液得到Al(OH)3固体 |
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
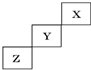

| A、X、Y、Z三种元素中,X的非金属性最强 |
| B、Y的氢化物的稳定性比Z的强 |
| C、Y的最高正化合价为+7价 |
| D、X的单质的熔点比Z的高 |
短周期金属元素甲~戊在周期表中的相对位置如下表所示,下面判断不正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、原子半径:丙<丁<戊 |
| B、金属性:甲<丙 |
| C、氢氧化物碱性:丙>丁>戊 |
| D、最外层电子数:甲>乙 |
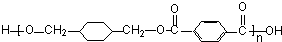
 -CH3+Cl2→
-CH3+Cl2→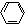 -CH2Cl+HCl
-CH2Cl+HCl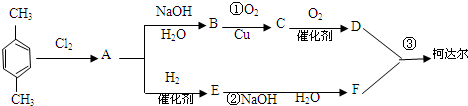
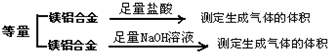
 为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究.请回答下列问题:
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究.请回答下列问题: