��Ŀ����
8����һ��ɫ��ĩ��������NaOH��K2SO4��CuSO4��Ba��OH��2��CaCO3��BaCl2�е�һ�ֻ�����ɣ���������ʵ�飺��1�����ĩ�м�������ˮ������ܽ����ˣ��ð�ɫ��������ɫ��Һ���ó���������CaCO3��BaSO4��ԭ��ĩһ������CuSO4��
��2����1���г��������������ᣬ���������ܽ⣬������ɫ���壮ԭ��ĩһ������CaCO3��K2SO4����Ӧ�����ӷ���ʽΪCaCO3+2H+=CO2��+H2O+Ca2+��
��3��ȡ��1���е���Һ��ͨ��������2���в��������壬�ֲ�����ɫ���������˵���Һ����1���е���Һһ������Ba2+��OH-���ӣ�
��4��ȡ��3���еõ�����Һ����AgNO3��Һ��ϡ���ᣬ�ֲ�����ɫ���������ӷ�Ӧ����ʽΪAg++Cl-=AgCl����ԭ��ĩ��һ������K2SO4��CaCO3��BaCl2�����ٺ���NaOH��Ba��OH��2�е�һ�֣�
���� ��һ��ɫ��ĩ��������NaOH��K2SO4��CuSO4��Ba��OH��2��CaCO3��BaCl2�е�һ�ֻ�����ɣ���������ʵ�飺
��1�����ĩ�м�������ˮ������ܽ����ˣ��ð�ɫ��������ɫ��Һ��ԭ�����к��в��ܵ�̼��ƣ�����BaCl2��Ba��OH��2������K2SO4��CuSO4�������ᱵ������������ҺΪ��ɫ����һ������CuSO4��
��3����2���в���������ΪCO2��ͨ�루1���е���Һ�ֲ�����ɫ�������˳���Ϊ̼�ᱵ����֪��Һ��������������
��4��ȡ��3���еõ�����Һ����AgNO3��Һ��ϡ���ᣬ�ֲ�����ɫ�������˳���Ϊ�Ȼ�����
��� �⣺��1�����ĩ�м�������ˮ������ܽ����ˣ��ð�ɫ�������ó��������Ƿ�Ӧ���ɵ�BaSO4��Ҳ������ԭ�����к��в��ܵ�̼��ƣ�ͬʱ����ɫ��Һ��˵������CuSO4���ʴ�Ϊ��CaCO3��BaSO4��CuSO4��
��2����1����������Ϊ̼��ƺ����ᱵ�������������ᣬ���������ܽ⣬�ܽ�ij���Ϊ̼��ƣ�������ɫ����Ϊ������̼�����ܵij���Ϊ���ᱵ����֪ԭ������һ����CaCO3��K2SO4���ܽ����ʱ������Ӧ�����ӷ���ʽΪCaCO3+2H+=CO2��+H2O+Ca2+��
�ʴ�Ϊ��CaCO3��K2SO4��CaCO3+2H+=CO2��+H2O+Ca2+��
��3����1���е���Һͨ��CO2���õ�̼�ᱵ��ɫ��������֪��Һ����Ba2+��OH-��
�ʴ�Ϊ��Ba2+��OH-��
��4��ȡ��3���еõ�����Һ����AgNO3��Һ��ϡ���ᣬ�ֲ���AgCl��ɫ���������������ӷ�ӦΪAg++Cl-=AgCl������֪��Һ�к���Cl-���������һ������K2SO4��CaCO3��BaCl2��NaOH��Ba��OH��2�����ٺ���һ�֣�
�ʴ�Ϊ��Ag++Cl-=AgCl����K2SO4��CaCO3��BaCl2��NaOH��Ba��OH��2��
���� �����������ƶ��⣬��ѧ���������⼰�����������������кܴ�İ������ڽ������ʱ�����ȷ���������и����ʵ����ʣ�Ȼ�������е�����������ڻ��ڵ����ʣ����ԭ����֤���ɣ�

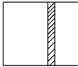 �����£�a mol A��b mol B����ͼ��ʾ���������ɻ����������з������·�Ӧ��A��g��+2B��g��?2C��g����һ��ʱ���ﵽƽ�⣬����n mol C��������˵������ȷ���ǣ�������
�����£�a mol A��b mol B����ͼ��ʾ���������ɻ����������з������·�Ӧ��A��g��+2B��g��?2C��g����һ��ʱ���ﵽƽ�⣬����n mol C��������˵������ȷ���ǣ�������| A�� | ����A��B��ת����֮��Ϊa��b | |
| B�� | ��ʼʱ�̺ʹ�ƽ��������е�ѹǿ��Ϊ��a+b������a+b-$\frac{n}{2}$�� | |
| C�� | ����ʼʱ����2a mol A��2b mol B�����ƽ��ʱ����2n mol C | |
| D�� | ��v����A��=2v����B��ʱ�����ж���Ӧ�ﵽƽ�� |
| A�� |  �μ�Һ��ҩƷ | B�� |  ���� | C�� |  ϡ��Ũ���� | D�� |  ��ȡҺ������ |
| A�� | ˮ��ƽ�������ƶ� | B�� | ����Ũ�Ⱦ���С | ||
| C�� | ��Һ��������Ŀ���� | D�� | c��Al3+����c��SO42-���ı�ֵ��С |
| A�� | Na2O����ˮ��Na2O+H2O=2Na++2OH- | |
| B�� | ��Ca��ClO��2��Һ��ͨ�����CO2��2ClO-+H2O+CO2=2HClO+CO32- | |
| C�� | ��FeCl3��Һ��ʴͭ�壺Fe3++Cu=Fe2++Cu2+ | |
| D�� | ̼�������ϡ���CaCO3+2H+=Ca2++CO2��+H2O |
 2NH3(g) ��H=-73kJ/mol
2NH3(g) ��H=-73kJ/mol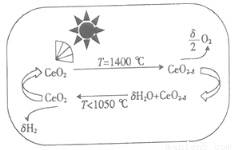
 +��Fe2+��Zn2+ B��ֻ�� Zn2+
+��Fe2+��Zn2+ B��ֻ�� Zn2+