题目内容
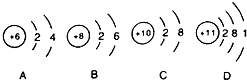
15.具有下列电子层结构的原子和离子,其对应元素一定属于同一周期的是( )| A. | 两原子N层上都有1个s电子,一个原子有d电子,另一个原子无d电子 | |
| B. | 最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子 | |
| C. | 原子核外M层上的s、p轨道都充满电子,而d轨道上没有电子的两种原子 | |
| D. | 两原子的核外全部都是s电子 |
分析 A.原子N层上都有1个s电子,原子无d电子为K原子,原子有d电子为Cr、Cu;
B.最外层电子排布为2s22p6的原子为氖原子,最外层电子排布为2s22p6的离子可能是阴离子也可能是阳离子;
C.原子核外M层上的s、p轨道都充满电子,而d轨道上没有电子,不能确定N层是否有电子排布,符合条件的原子为氩原子,钾原子,钙原子;
D.两原子的核外全部都是s电子,原子具有1s能级或具有1s、2s能级.
解答 解:A.原子N层上都有1个s电子,原子无d电子为K原子,原子有d电子为1s22s22p63s23p63d54s1,是Cr原子,1s22s22p63s23p63d104s1,是Cu原子,都处于第四周期,故A正确;
B.最外层电子排布为2s22p6的原子为氖原子,最外层电子排布为2s22p6的离子可能是阴离子也可能是阳离子如O2-、Na+等,不一定处于同一周期,故B错误;
C.原子核外M层上的s、p轨道都充满电子,而d轨道上没有电子,符合条件的原子的核外电子排布式有1s22s22p63s23p6为氩原子,1s22s22p63s23p64s1为钾原子,1s22s22p63s23p64s2为钙原子,不一定处于同一周期,故C错误;
D.两原子的核外全部都是s电子,原子具有1s能级或具有1s、2s能级,不处于同一周期,如氢原子与锂原子,故D错误;
故选A.
点评 本题考查核外电子排布规律,难度中等,掌握核外电子排布规律:①、每个轨道最多只能容纳两个电子,且自旋相反配对;②、能量最低原理:电子尽可能占据能量最低的轨道;③、简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子;另外:等价轨道在全充满、半充满或全空的状态是比较稳定的.

练习册系列答案
相关题目
3.下列说法不正确的是( )
| A. | 向煤中加入适量CaO,可大大减少燃烧产物中SO2的量 | |
| B. | 葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 | |
| D. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 |
10.下列反应在一定条件下可以完成的是( )
①非金属置换金属的反应
②弱酸可以生成强酸的反应
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应
⑤铜置换出氢气的反应.
①非金属置换金属的反应
②弱酸可以生成强酸的反应
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应
⑤铜置换出氢气的反应.
| A. | ①②③ | B. | ①②④ | C. | ②③④⑤ | D. | ①②③④⑤ |
7.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关.下列各组物质:
①Cu与HNO3溶液
②Cu与FeCl3溶液
③Zn与H2SO4溶液
④Fe与HCl溶液
⑤O2与Na,由于浓度不同而发生不同氧化还原反应的是( )
①Cu与HNO3溶液
②Cu与FeCl3溶液
③Zn与H2SO4溶液
④Fe与HCl溶液
⑤O2与Na,由于浓度不同而发生不同氧化还原反应的是( )
| A. | ①③ | B. | ③⑤ | C. | ①②⑤ | D. | ①③⑤ |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 工业采用火法炼铜:Cu2S+O2=2Cu+SO2 每生成2mol铜,反应共转移4NA个电子 | |
| B. | 7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.1NA | |
| C. | CO2通过Na2O2使其增重bg时,反应中转移的电子数为$\frac{b{N}_{A}}{44}$ | |
| D. | 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.02NA |
5.葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6$\stackrel{酵母}{→}$2CH3CH2OH+2CO2↑).
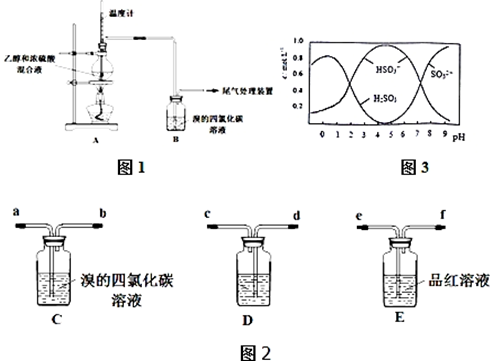
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
(1)溶液“渐渐变黑”,说明浓硫酸具有脱水性.
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp=1×10-10,Ksp=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全,此时溶液中c(SO32-)≤0.05mol•L-1.

Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp=1×10-10,Ksp=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全,此时溶液中c(SO32-)≤0.05mol•L-1.
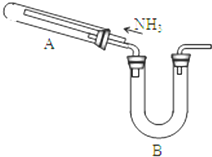 某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如图.
某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如图.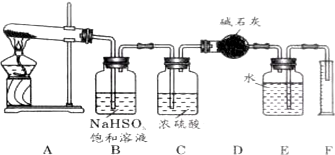
 推测硒在元素周期表中第四周期;
推测硒在元素周期表中第四周期;