题目内容
17.某有机物在O2中充分燃烧生成CO2和H2O的物质的量之比为1:1,下列结论正确的是( )| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物中肯定不含氧 | |
| C. | 该有机物分子中碳、氢原子个数比为1:2 | |
| D. | 该有机物中肯定含有氧 |
分析 该有机物生成的水和二氧化碳的物质的量比为1:1,所以可以据此可以求算出其中碳原子和氢原子的个数比,但是不能判断其中氧原子与碳原子及氢原子的个数比,然后结合质量守恒定律即可完成判断.
解答 解:A.有机物在O2中充分燃烧生成CO2和H2O的物质的量之比为1:1,根据质量守恒定律可以判断在有机物中含有碳原子和氢原子,但是不能判断出该有机物中是否含有氧元素,故A错误;
B.有机物的质量未给出,无法判断有机物中是否含有氧元素,故B错误;
C.该有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,根据原子守恒可知,有机物中分子中碳、氢原子个数比为1:2,故C正确;
D.有机物的质量未给出,无法判断有机物中是否含有氧元素,故D错误.
故选C.
点评 本题考查有机物分子式确定的计算与判断,题目难度中等,注意明确本题中利用原子守恒确定有机物分子中C、H原子个数之比,但不能确定是否含有氧元素.

练习册系列答案
相关题目
10.下列反应既是氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2的反应 | |
| C. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 | |
| D. | 甲烷在空气中燃烧的反应 |
8.下列原子结构示意图中,正确的是( )
| A. | 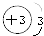 | B. |  | C. | 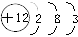 | D. | 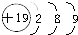 |
12.核电荷数为1~20的元素中,次外层电子数是最外电子层电子数4倍的元素共有( )
| A. | 4 种 | B. | 3 种 | C. | 2 种 | D. | l 种 |
2.下列说法正确的是( )
| A. | 含有离子键的化合物必是离子化合物 | |
| B. | 含有共价键的化合物就是共价化合物 | |
| C. | 共价化合物可能含离子键 | |
| D. | 离子化合物中一定含有共价键 |
9.下列说法不正确的是( )
| A. | 胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀 | |
| B. | 一种透明液体中加入电解质溶液,若有沉淀生成,则该液体不一定是胶体 | |
| C. | 光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应 | |
| D. | 放电影时,放映室射到银幕上的光柱是由胶粒对光的散射形成的 |
6.下列食物中,属于碱性食物的是( )
| A. | 鸡蛋 | B. | 牛肉 | C. | 鱼 | D. | 黄瓜 |
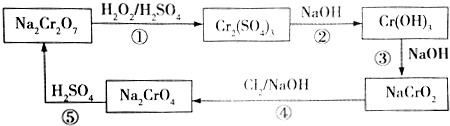
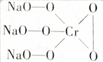 ,则Cr的化合价为+5,其中含有的化学键有离子键、共价键.
,则Cr的化合价为+5,其中含有的化学键有离子键、共价键.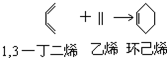
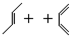 →
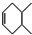
→
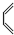 +
+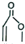 →
→