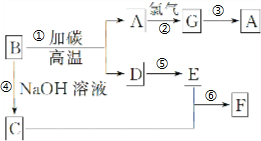
题目内容
完成以下几步转化的化学方程式,除⑥外,其他的还要写出离子方程式.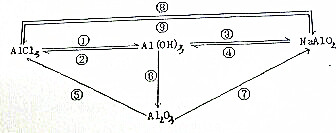

考点:镁、铝的重要化合物,化学方程式的书写
专题:几种重要的金属及其化合物
分析:①为氯化铝与氨水反应生成氢氧化铝沉淀和氯化铵,②为氢氧化铝与盐酸反应生成氯化铝和水,③为氢氧化铝与NaOH的反应生成偏铝酸钠和水,④为偏铝酸钠与过量二氧化碳的反应,⑤为氧化铝与盐酸反应生成氯化铝和水,⑥为氢氧化铝的分解反应,⑦为氧化铝与NaOH反应生成偏铝酸钠和水,⑧为氯化铝与过量氢氧化钠反应生成偏铝酸钠和水,⑨为偏铝酸钠与过量盐酸的反应,以此来解答.
解答:
解:①为氯化铝与氨水反应生成氢氧化铝沉淀和氯化铵,化学方程式为:AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl;离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
②为氢氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O;离子方程式为:Al(OH)3+3H+=Al3++3H2O;
③为氢氧化铝与NaOH的反应生成偏铝酸钠和水,化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O;离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
④为偏铝酸钠与过量二氧化碳的反应,化学方程式为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
⑤为氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al2O3+6HCl=2AlCl3+3H2O;离子方程式为:Al2O3+6H+=2Al3++3H2O;
⑥为氢氧化铝的分解反应,化学方程式为:2Al(OH)3
Al2O3+3H2O,
⑦为氧化铝与NaOH反应生成偏铝酸钠和水,化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O;离子方程式为:Al2O3+2OH-=2AlO2-+H2O;
⑧为氯化铝与过量氢氧化钠反应生成偏铝酸钠和水,化学方程式为:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O;离子方程式为:Al3++4OH-=AlO2-+2H2O;
⑨为偏铝酸钠与过量盐酸的反应,化学方程式为:NaAlO2+4HCl=AlCl3+NaCl+2H2O;离子方程式为:AlO2-+4H+=Al3++2H2O;
答:①AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl、Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
②Al(OH)3+3HCl=AlCl3+3H2O、Al(OH)3+3H+=Al3++3H2O;
③Al(OH)3+NaOH=NaAlO2+2H2O、Al(OH)3+OH-=AlO2-+2H2O;
④NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3、AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
⑤Al2O3+6HCl=2AlCl3+3H2O、Al2O3+6H+=2Al3++3H2O;
⑥2Al(OH)3
Al2O3+3H2O,
⑦Al2O3+2NaOH=2NaAlO2+H2O、Al2O3+2OH-=2AlO2-+H2O;
⑧AlCl3+4NaOH=NaAlO2+3NaCl+2H2O、Al3++4OH-=AlO2-+2H2O;
⑨NaAlO2+4HCl=AlCl3+NaCl+2H2O、AlO2-+4H+=Al3++2H2O.
②为氢氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O;离子方程式为:Al(OH)3+3H+=Al3++3H2O;
③为氢氧化铝与NaOH的反应生成偏铝酸钠和水,化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O;离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
④为偏铝酸钠与过量二氧化碳的反应,化学方程式为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
⑤为氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al2O3+6HCl=2AlCl3+3H2O;离子方程式为:Al2O3+6H+=2Al3++3H2O;
⑥为氢氧化铝的分解反应,化学方程式为:2Al(OH)3
| ||
⑦为氧化铝与NaOH反应生成偏铝酸钠和水,化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O;离子方程式为:Al2O3+2OH-=2AlO2-+H2O;
⑧为氯化铝与过量氢氧化钠反应生成偏铝酸钠和水,化学方程式为:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O;离子方程式为:Al3++4OH-=AlO2-+2H2O;
⑨为偏铝酸钠与过量盐酸的反应,化学方程式为:NaAlO2+4HCl=AlCl3+NaCl+2H2O;离子方程式为:AlO2-+4H+=Al3++2H2O;
答:①AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl、Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
②Al(OH)3+3HCl=AlCl3+3H2O、Al(OH)3+3H+=Al3++3H2O;
③Al(OH)3+NaOH=NaAlO2+2H2O、Al(OH)3+OH-=AlO2-+2H2O;
④NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3、AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
⑤Al2O3+6HCl=2AlCl3+3H2O、Al2O3+6H+=2Al3++3H2O;
⑥2Al(OH)3
| ||
⑦Al2O3+2NaOH=2NaAlO2+H2O、Al2O3+2OH-=2AlO2-+H2O;
⑧AlCl3+4NaOH=NaAlO2+3NaCl+2H2O、Al3++4OH-=AlO2-+2H2O;
⑨NaAlO2+4HCl=AlCl3+NaCl+2H2O、AlO2-+4H+=Al3++2H2O.
点评:本题考查化学反应的书写,为高频考点,把握物质的性质及转化为解答的关键,侧重化学用语的考查,题目难度不大.

练习册系列答案
相关题目
1977年在印度洋东南部马德里斯的一个海湾里,一阵飓风过后,海面的巨浪上竟燃烧着熊熊大火.海水会燃烧的原因是( )
| A、时速达280公里的飓风与海水发生剧烈摩擦,产生的巨大热能使水分子分解,引起氢气燃烧 |
| B、飓风使海水分子运动速度加快,产生的热能使海水中植物燃烧 |
| C、海面上漂浮的油层被氧化而燃烧 |
| D、以上叙述都正确 |
向淀粉中加入少量的稀硫酸,加热使之发生水解,为测定水解的程度所需下列试剂是( )
①NaOH溶液 ②新制Cu(OH)2溶液 ③碘水 ④BaCl2溶液.
①NaOH溶液 ②新制Cu(OH)2溶液 ③碘水 ④BaCl2溶液.
| A、②③ | B、①②③ |
| C、①②④ | D、②③④ |
下列有关实验原理或操作,正确的是( )
| A、镀层未破损的镀锌铁和镀层破损后的镀锌铁分别与盐酸反应时产生H2的速度相同 |
| B、用50mL酸式滴定管可准确量取25.00mL的Na2CO3溶液 |
| C、往新配制的淀粉溶液中滴加碘水,溶液显蓝色,加入足量NaOH后溶液褪色 |
| D、配制稀H2SO4溶液时,先在量筒中加入一定体积的水,再在不断搅拌下慢慢加浓H2SO4 |
下列物质中,能用来干燥H2的是( )
| A、NaHCO3 |
| B、Na2O2 |
| C、Na2CO3 |
| D、NaOH |


 是E的最简单的同系物,试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件)
是E的最简单的同系物,试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件) 某有机物A,由C、H、O三种元素组成,在一定条件下,有以下转变关系:(R-CH2CH2OH
某有机物A,由C、H、O三种元素组成,在一定条件下,有以下转变关系:(R-CH2CH2OH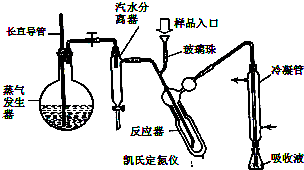 蛋白质是有机态氮的表现形式之一,蛋白质样品(或其他含氮杂质)与硫酸和催化剂一同加热消化,使含氮物质分解,分解成的氨与硫酸结合生成硫酸铵,然后碱化蒸馏使氨游离,用硼酸吸收后再用盐酸标准溶液滴定,根据酸的消耗量求得氮的质量分数,乘以换算系数(奶粉中为6.25),即得蛋白质含量.
蛋白质是有机态氮的表现形式之一,蛋白质样品(或其他含氮杂质)与硫酸和催化剂一同加热消化,使含氮物质分解,分解成的氨与硫酸结合生成硫酸铵,然后碱化蒸馏使氨游离,用硼酸吸收后再用盐酸标准溶液滴定,根据酸的消耗量求得氮的质量分数,乘以换算系数(奶粉中为6.25),即得蛋白质含量. ) B.样品入口未用蒸馏水冲洗
) B.样品入口未用蒸馏水冲洗