��Ŀ����
��֪A��B��C��D���Ƕ�����Ԫ�أ����ǵ�ԭ�Ӱ뾶��СΪB��C��D��A��B�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ��Dԭ����2��δ�ɶԵ��ӡ�A��B��D����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����塣E�ǵ�������Ԫ�أ���ԭ�Ӻ���������������Aԭ����ͬ�����������Ӿ��������ش��������⣨��Ԫ�ط��Ż�ѧʽ��ʾ����
��1��M������Bԭ�ӹ�����ӻ�����Ϊ ��
��2��������CA3�ķе�Ȼ�����BA4�ĸߣ�����Ҫԭ���� ��
��3��д����BD2��Ϊ�ȵ������C3���Ľṹʽ ��
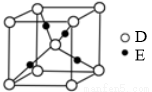
��4��E+�ĺ�������Ų�ʽΪ ����ͼ��D��E�γɵ�ij�ֻ�����ľ����ṹʾ��ͼ���þ���1�������������ӵĸ���Ϊ ��
��5����E����������Һ��ͨ�������CA3��������[E(CA3)4]2+�����ӣ�1 mol [E(CA3)4]2+�к��ЦҼ�����ĿΪ ��
��1��sp2 ��2��NH3���Ӽ����γ���� ��3��[N=N=N]-
��4��1s22s22p63s23p63d10 4
��5��16mol����16��6.02��1023��
��������
�����������������֪��B�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ����BΪ̼Ԫ�أ�Dԭ����2��δ�ɶԵ��ӣ�A��B��D����Ԫ����ɵ�һ�ֻ�����MΪ��ȩ��ԭ�Ӱ뾶��СΪB��C��D��A����AΪ��Ԫ�أ�DΪ��Ԫ�أ�CΪ��Ԫ�أ� E�ǵ�������Ԫ�أ���ԭ�Ӻ���������������Aԭ����ͬ�����������Ӿ���������EΪͭԪ�ء���1����ȩ�ĽṹʽΪ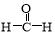 ��������̼Ԫ��ԭ�ӹ�����ӻ�����Ϊsp2����2��������NH3�ķе�Ȼ�����CH4�ĸߣ�����Ҫԭ����NH3���Ӽ����γ��������3����CO2��Ϊ�ȵ������N3���ĽṹʽΪ[N=N=N]-����4��ͭΪ29��Ԫ�أ�Cu+�ĺ�������Ų�ʽΪ1s22s22p63s23p63d10������O��Cu�γɵ�ij�ֻ�����ľ����ṹʾ��ͼ���÷�̯��ȷ�����þ���1�������������ӵĸ���Ϊ8��1/8+1=2����5��������ͭ��Һ��ͨ�������NH3��������[Cu (NH3)4]2+�����ӣ���[Cu(NH3)4]2+���ĸ�NH3ͨ����λ����Cu2+��ϣ���ÿ��NH3�к���3�����ۼ���������������[Cu(NH3)4]2+�к��еĹ��ۼ�Ϊ3��4+4=16.���1mol��������к��ЦҼ�����ĿΪ16mol����16��6.02��1023����
��������̼Ԫ��ԭ�ӹ�����ӻ�����Ϊsp2����2��������NH3�ķе�Ȼ�����CH4�ĸߣ�����Ҫԭ����NH3���Ӽ����γ��������3����CO2��Ϊ�ȵ������N3���ĽṹʽΪ[N=N=N]-����4��ͭΪ29��Ԫ�أ�Cu+�ĺ�������Ų�ʽΪ1s22s22p63s23p63d10������O��Cu�γɵ�ij�ֻ�����ľ����ṹʾ��ͼ���÷�̯��ȷ�����þ���1�������������ӵĸ���Ϊ8��1/8+1=2����5��������ͭ��Һ��ͨ�������NH3��������[Cu (NH3)4]2+�����ӣ���[Cu(NH3)4]2+���ĸ�NH3ͨ����λ����Cu2+��ϣ���ÿ��NH3�к���3�����ۼ���������������[Cu(NH3)4]2+�к��еĹ��ۼ�Ϊ3��4+4=16.���1mol��������к��ЦҼ�����ĿΪ16mol����16��6.02��1023����
���㣺�������ʽṹ�����ʡ�

 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д� һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�A��������������γɻ��漰��Ӧ��2H2SO3+O2
| ||||
| B����������ˮ�п��γɴ������Al��OH��3������Al3++3H2O?Al��OH��3�����壩+3H+ | ||||
| C��ѡ��CuSO4��Һ��ȥ��Ȳ�����е�H2S��H2S+Cu2+�TCuS��+2H+ | ||||
| D���ȵĴ���Һ������ϴ���۵�ԭ��CO32?+2H2O?H2CO3+2OH? |
 C2H5OH(g) ��H�� ��
C2H5OH(g) ��H�� ��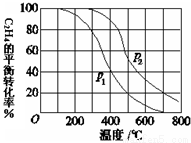
 Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25��
Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25��

 BaSO4��
BaSO4��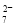 ��ԭΪCr3������ͨ�����ڷ�ˮ��pH��ʹ��������ɷ���������������(Fe3O4��Fe2O3��FeO)�ĸ���������(
��ԭΪCr3������ͨ�����ڷ�ˮ��pH��ʹ��������ɷ���������������(Fe3O4��Fe2O3��FeO)�ĸ���������(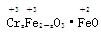 )��������1 mol Cr2O
)��������1 mol Cr2O