题目内容
下列说法正确的是( )
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 615.3 | 414.4 | 347.4 | 435.3 |
| A、已知则可以计算CH3-CH3(g)→CH2=CH2(g)+H2(g)△H=+125.6 kJ/mol |
| B、容量瓶、量筒和滴定管上都要标明使用温度,容量瓶无“0”刻度,量筒、滴定管都有“0”刻度;使用时量筒和滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| C、氯化镁溶液与氨水反应:Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+ |
| D、使石蕊呈紫色的溶液中,下列离子可以大量共存:Na+、AlO2-、NO3-、HCO3- |
考点:离子共存问题,有关反应热的计算
专题:离子反应专题,化学反应中的能量变化
分析:A.根据反应热等于反应物总键能减生成物总键能计算;
B.量筒没有0刻度;
C.氯化镁溶液与氨水反应生成氢氧化镁和氯化铵;
D.石蕊呈紫色的溶液呈中性,水解呈碱性的离子不能大量共存.
B.量筒没有0刻度;
C.氯化镁溶液与氨水反应生成氢氧化镁和氯化铵;
D.石蕊呈紫色的溶液呈中性,水解呈碱性的离子不能大量共存.
解答:
解:A.在反应CH3-CH3→CH2=CH2+H2中,断裂6mol C-H键,1mol C-C键共吸收的能量为:6×414.4kJ+347.4kJ=2833.8kJ,
生成1molCH2=CH2和1molH2,共形成4molC-H键,1molC=C、1molH-H,共放出的能量为:4×414.4kJ+615.3kJ+435.3kJ=2708.2kJ,
吸收的能量多,放出的能量少,该反应为吸热反应,吸收的热量为:2833.8kJ-2708.2kJ=125.6,所以反应热为+125.6kJ/mol,
则热化学方程式为CH3-CH3(g)→CH2=CH2(g)+H2(g)△H=+125.6 kJ/mol,故A正确;
B.量筒没有0刻度,且无需润洗,故B错误;
C.氯化镁溶液与氨水反应生成氢氧化镁和氯化铵,反应的离子方程式为Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+,故C正确;
D.AlO2-、HCO3-水解呈碱性,不可能存在中性溶液中,故D错误.
故选AC.
生成1molCH2=CH2和1molH2,共形成4molC-H键,1molC=C、1molH-H,共放出的能量为:4×414.4kJ+615.3kJ+435.3kJ=2708.2kJ,
吸收的能量多,放出的能量少,该反应为吸热反应,吸收的热量为:2833.8kJ-2708.2kJ=125.6,所以反应热为+125.6kJ/mol,
则热化学方程式为CH3-CH3(g)→CH2=CH2(g)+H2(g)△H=+125.6 kJ/mol,故A正确;
B.量筒没有0刻度,且无需润洗,故B错误;
C.氯化镁溶液与氨水反应生成氢氧化镁和氯化铵,反应的离子方程式为Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+,故C正确;
D.AlO2-、HCO3-水解呈碱性,不可能存在中性溶液中,故D错误.
故选AC.
点评:本题考查较为综合,涉及化学反应与能量、定量仪器的使用、离子方程式以及离子共存问题,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握题给信息以及相关基础知识的积累,难度不大.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
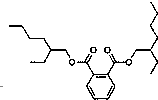 曾引起台湾地区食品安全轩然大波的塑化剂的分子结构如图所示:下列叙述中不正确的是( )
曾引起台湾地区食品安全轩然大波的塑化剂的分子结构如图所示:下列叙述中不正确的是( )| A、该物质的分子式为C24H38O4 |
| B、该物质属于酯类,不溶于水 |
| C、该物质能与溴水发生加成反应 |
| D、该物质发生水解反应,其生成的醇只有一种 |
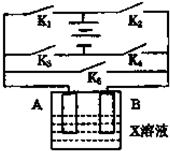 某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液
某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| A、甲同学在实验中将开关K5闭合,Zn电极上产生气泡 |
| B、乙同学打算闭合K3、K4做电解CuCl2溶液的实验 |
| C、乙同学用淀粉碘化钾试纸检验电解产生的氯气 |
| D、丙同学准备在Fe上镀Cu,选择了一种铜盐来配制电镀液,闭合的开关的组合是K2、K3 |
在实验室里,要想使AlCl3中的Al3+全部沉淀出来,应选用下列试剂中的( )
| A、石灰水 | B、氢氧化钠溶液 |
| C、硫酸 | D、氨水 |
 图1和图2分别是1s电子的概率分布图和原子轨道图.下列有关认识正确的是( )
图1和图2分别是1s电子的概率分布图和原子轨道图.下列有关认识正确的是( )| A、图1中的每个小黑点表示1个电子 |
| B、图2表示1s电子只能在球体内出现 |
| C、图2表明1s轨道呈圆形,有无数对称轴 |
| D、图1中的小黑点表示某一时刻,电子在核外所处的位置 |
某可逆反应a A(g)+bB(g)?cC(g),在温度分别为T1和T2,压强分别为P1和P2条件下,得到C的物质的量n与时间t的关系曲线如下图所示.据图分析,以下正确的是( )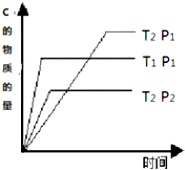

| A、c>a+b,正反应为吸热反应 |
| B、c>a+b,正反应为放热反应 |
| C、c<a+b,逆反应为吸热反应 |
| D、c<a+b,逆反应为放热反应 |
如图物质一定属于同系物的是( )
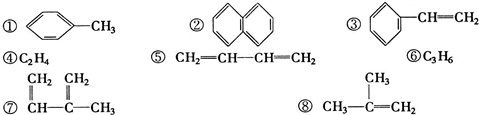

| A、①和②、④和⑥ |
| B、⑤和⑦、④和⑧ |
| C、④和⑥、⑤和⑦ |
| D、④和⑥、⑧ |
在标准状况下,若V L甲烷中含有的氢原子个数为n,则阿伏加德罗常数可表示为( )
| A、5.6 n/V |
| B、22.4 n/V |
| C、V n/5.6 |
| D、V n/22.4 |
下列物质中,所含分子数目相同的是( )
| A、10 g H2和10 g O2 |
| B、5.6 LN2(标准状况)和11 g CO2 |
| C、9 g H2O和11.2 L(标准状况)苯 |
| D、224 mL H2(标准状况)和0.1 mol N2 |