题目内容
5.SO2用氢氧化钠溶液吸收后可得到Na2SO3溶液,再用Na2SO3溶液和单质硫共热可制备海波(Na2S2O3),其总反应的化学方程式为Na2SO3+S$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3,海波也可用Na2S和Na2SO3反应制备,制备时,参加反应的Na2S和Na2SO3的物质的量之比为2Na2S+3SO2+Na2SO3=3Na2S2O3.分析 用Na2SO3溶液和单质硫共热可制备海波(Na2S2O3),海波也可用Na2S和Na2SO3反应制备,制备时需要通入二氧化硫发生氧化还原反应,参加反应的Na2S和Na2SO3的物质的量之比依据化学方程式定量关系得到.
解答 解:用Na2SO3溶液和单质硫共热可制备海波(Na2S2O3),反应的总化学方程式为:Na2SO3+S$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3,海波也可用Na2S和Na2SO3反应制备,制备时需要通入二氧化硫发生氧化还原反应,参加反应的Na2S和Na2SO3的物质的量之比依据化学方程式定量关系得到:2Na2S+3SO2+Na2SO3=3Na2S2O3,
故答案为:Na2SO3+S$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3 ;2Na2S+3SO2+Na2SO3=3Na2S2O3.
点评 本题考查了二氧化硫性质、化学方程式书写、产物和反应物判断,掌握基础是解题关键,题目难度中等.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 标准状况下,22.4 L N2和CO2混合气体所含的分子数为2NA | |
| C. | 1 L浓度为1 mol•L-1的 H2O2水溶液中含有的氧原子数为2NA | |
| D. | MnO2和浓盐酸反应生成1 mol氯气时,转移的电子数为2NA |
13.下列实验操作能达到目的是( )
| A. | 加热氯化铵固体制取氨气 | |
| B. | 检验乙醇中是否含水:用无水硫酸铜,观察是否变蓝色 | |
| C. | 除去乙醛中的乙酸杂质:加入氢氧化钠溶液洗涤,分液 | |
| D. | 滴有酚酞的碳酸钠中,加入氯化钡溶液后,红色变浅,证明碳酸钠溶液中存在水解平衡 |
20.NA表示阿伏加德罗常数.下列叙述正确的是( )
| A. | 通常状况下,1mol/L Na2CO3溶液中含钠离子数为2NA | |
| B. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| C. | 1mol N5+含有的电子数为34NA | |
| D. | 1mol NH4+中含有的中子数为10NA |
10.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 62g白磷中含有2NA个白磷分子 | |
| B. | 1L 0.2mol/L Ba(NO3)2溶液中含有0.2NA个NO3- | |
| C. | 标准状况下,用MnO2和浓盐酸反应制取Cl2,当有4mol HCl被氧化时,生成2NA Cl2 | |
| D. | 25℃时,pH=7的NH4Cl和NH3•H2O的混合溶液中,0H-数10-7NA |
4.某元素的一种同位素原子${\;}_{Z}^{A}$X,它与3H原子组成HmX分子,在agHmX中所含中子的物质的量是( )
| A. | $\frac{a}{A}$(A-Z+2m)mol | B. | $\frac{a}{A}$(A+2m)mol | C. | $\frac{a}{A+3m}$(A-Z+3m)mol | D. | $\frac{a}{A+3m}$(A-Z+2m)mol |
1.分子式为C5H12O的所有醇中,被氧化后可产生饱和一元醛最多有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
2.Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中的一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.4g,下列分析正确的是( )
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | C. | 可能含有NaHCO3 | D. | 一定含有NaCl |
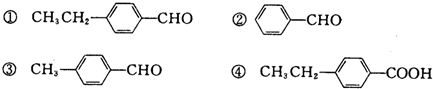
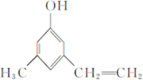 .
.