题目内容
17.将10mL 3mol/L的盐酸与10mL 1mol/L的CaCl2溶液混合,则混合溶液中Cl-的物质的量浓度是多少?(设混合后溶液的体积不变)分析 结合n=cV及物质构成计算Cl-的物质的量,再结合c=$\frac{n}{V}$计算浓度.
解答 解:混合溶液中Cl-的物质的量为0.01L×3mol/L+0.01L×1mol/L×2=0.05mol,溶液总体积为0.02L,则混合溶液中Cl-的物质的量浓度是$\frac{0.05mol}{0.02L}$=2.5mol/L,
答:混合溶液中Cl-的物质的量浓度是2.5mol/L.
点评 本题考查物质的量浓度的计算,为高频考点,把握物质的量与浓度的关系为解答的关键,侧重分析与计算能力的考查,注意溶液体积的判断,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
20.下列属于加成反应的是( )
| A. | 乙烯通入溴水中使溴水褪色 | |
| B. | 乙烯使酸性高锰酸钾溶液褪色 | |
| C. | 四氯化碳与溴水混合振荡,静置后溴水褪色 | |
| D. | 乙烷与Cl2光照条件下反应 |
8.下列能达到实验目的是( )
| A. | 在量筒中加入一体积的水,再加入浓硫酸配制稀硫酸 | |
| B. | 用澄清石灰水检验CO中含有的CO2 | |
| C. | 用玻璃棒搅拌漏斗中的液体以加快过滤速度 | |
| D. | 加入盐酸以除去硫酸钠中的少许碳酸钠杂质 |
12.在标准状况下,相同质量的下列气体体积最小的是( )
| A. | O2 | B. | CO2 | C. | H2 | D. | SO2 |
2.有一种无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的一种或几种.为确定其成分,进行如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入过量的Na2O2固体后白色沉淀部分溶解,②另取部分溶液,加入HCl酸化的BaCl2溶液,有白色沉淀产生.下列推断正确的是( )
| A. | 肯定有Al3+、Mg2+、Cl- | B. | 肯定有Al3+、Mg2+、NH4+、Cl- | ||
| C. | 肯定有HCO3-、K+、MnO4- | D. | 肯定有Al3+、Mg2+、SO42- |
6.下列有关物质用途的说法中,不正确的是( )
| A. | 氯气可做自来水消毒剂 | B. | 碳酸钠可用于制造玻璃制造肥皂 | ||
| C. | 二氧化硅可用于制造集成电路 | D. | Na2O2用作潜水艇供氧剂 |
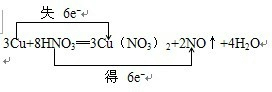 ,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.
,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.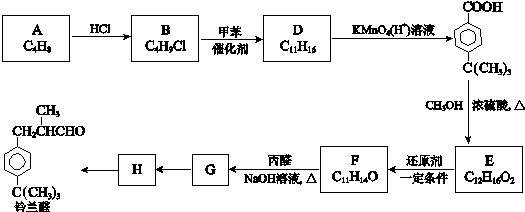
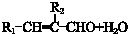
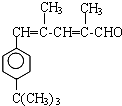
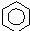 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ 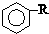 +HCl
+HCl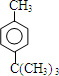 .
.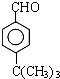 .
.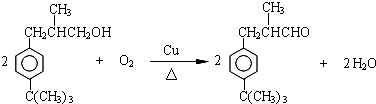 .
. .
.