题目内容
在容积相等的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol和b mol HI(a>b),发生反应2HI(g)?H2(g)+I2(g)达到平衡后,下列说法中,正确的是( )
| A、从开始反应到达平衡,所需时间tA>tB |
| B、平衡时,I2蒸气在混合气体中的体积分数φA>φB |
| C、平衡时,I2蒸气的物质的量浓度[I2]A=[I2]B |
| D、HI的平衡转化率,αA=αB |
考点:化学平衡的计算
专题:
分析:恒温恒容条件下,同时向A、B中分别加入a mol和b mol HI(a>b),发生反应2HI(g)?H2(g)+I2(g)达到平衡后,建立的平衡为等效平衡,各组分的体积分数相等,HI的转化率相等,由于a>b,A中浓度大,反应速率快,达到平衡所需时间少,平衡时,I2蒸气的物质的量浓度[I2]A>[I2]B,
A、容器中A中反应物的浓度大,反应速率大;
B、平衡为等效平衡,I2蒸气在混合气体中的体积分数φA=φB;
C、平衡时,I2蒸气的物质的量浓度[I2]A>[I2]B;
D、平衡为等效平衡,两容器中平衡时HI的转化率相同.
A、容器中A中反应物的浓度大,反应速率大;
B、平衡为等效平衡,I2蒸气在混合气体中的体积分数φA=φB;
C、平衡时,I2蒸气的物质的量浓度[I2]A>[I2]B;
D、平衡为等效平衡,两容器中平衡时HI的转化率相同.
解答:
解:A、容器中A中反应物的浓度大,反应速率大,达平衡需要的时间少,故A错误;
B、恒温恒容,反应2HI(g)?H2(g)+I2(g)达到平衡后,建立的平衡为等效平衡,I2蒸气在混合气体中的体积分数φA=φB,故B错误;
C、a>b,平衡时,A容器中各物质的浓度比B容器中各物质的浓度大,故C错误;
D、平衡为等效平衡,两容器中平衡时HI的转化率相同,故D正确.
故选:D.
B、恒温恒容,反应2HI(g)?H2(g)+I2(g)达到平衡后,建立的平衡为等效平衡,I2蒸气在混合气体中的体积分数φA=φB,故B错误;
C、a>b,平衡时,A容器中各物质的浓度比B容器中各物质的浓度大,故C错误;
D、平衡为等效平衡,两容器中平衡时HI的转化率相同,故D正确.
故选:D.
点评:本题考查了反应前后气体体积不变的化学反应的等效平衡,在达到平衡时的各组分的百分含量相等,但反应速率有区别,浓度越大,反应速率越快.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
下列材料不属于铁合金的是( )
| A、塑钢门窗 | B、不锈钢餐具 |
| C、钢化玻璃 | D、汽车底架 |
下列物质属于纯净物的是( )
| A、漂白粉 | B、盐酸 | C、氯水 | D、液溴 |
向一直充满水且倒立与水槽中的大试管中依次通入V1 ml NO2、V2 ml O2、V3ml NO,最后试管中充满溶液.则V1、V2、V3的比值可能为( )
①1:1:1 ②6:3:2 ③2:5:6 ④8:5:4.
①1:1:1 ②6:3:2 ③2:5:6 ④8:5:4.
| A、① | B、①② |
| C、①②③ | D、都有可能 |
将CO2和C加入密闭容器中,在一定条件下发生反应:CO2(g)+C(s)?2CO(g),忽略固体体积,平衡时CO的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是( )
| 温度/℃ CO的体积分数/% 压强/MPa | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 80.0 |
| A、b<f |
| B、900℃,2.0MPa的转化率为60% |
| C、K(1000℃)=3.2 |
| D、K(1000℃)>K(800℃) |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C、Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
| D、FeCl2溶液:K+、Na+、SO42-、AlO2- |
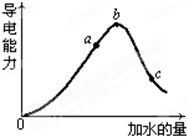 (1)a、b、c三点中醋酸的电离程度最大的是
(1)a、b、c三点中醋酸的电离程度最大的是