题目内容
向0.1mol?L-1 NaOH溶液中加入0.1mol?L-1的盐酸.若用x代表加入盐酸的体积,y代表溶液中离子的总数,则下列曲线中正确的是( )
A、 |
B、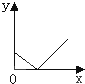 |
C、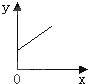 |
D、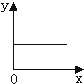 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:图示题,电离平衡与溶液的pH专题
分析:氢氧化钠的电离方程式为:NaOH=OH-+Na+,HCl的电离方程式为:HCl=Cl-+H+,在加入盐酸的过程中,发生反应的离子方程式为:OH-+H+═H2O,即加入的氢离子与氢氧根离子反应,加入氯离子与溶液中减少的氢氧根离子数目相等,即二者恰好反应前溶液中离子总数基本不变;当两溶液恰好反应后,盐酸过量,溶液中离子总数会逐渐增多.
解答:
解:NaOH和HCl都是一元的强电解质,其电离方程式分别为:NaOH=OH-+Na+、HCl=Cl-+H+,
加入盐酸的过程中,发生反应:OH-+H+═H2O,由于减少的氢氧根离子=溶液中增加的Cl-离子,则两溶液恰好反应之前,溶液中离子总数不变,
当氢氧化钠与盐酸恰好反应后,再加入盐酸,溶液中盐酸过量,导致离子总数逐渐增多,
根据以上分析可知,满足变化的图象为A,
故选A.
加入盐酸的过程中,发生反应:OH-+H+═H2O,由于减少的氢氧根离子=溶液中增加的Cl-离子,则两溶液恰好反应之前,溶液中离子总数不变,
当氢氧化钠与盐酸恰好反应后,再加入盐酸,溶液中盐酸过量,导致离子总数逐渐增多,
根据以上分析可知,满足变化的图象为A,
故选A.
点评:本题考查了离子反应方程式的应用,题目难度中等,注意明确氢氧化钠与盐酸反应的实质,正确理解题干选项“y代表溶液中离子的总数”是解答本题的关键.

练习册系列答案
相关题目
下列叙述不正确的是( )
| A、苯与氢气反应属于加成反应 |
| B、苯与硝酸的反应是加成反应 |
| C、苯与液溴生成溴苯 |
| D、苯能够萃取溴水中的溴 |
把11克金属混合物加入足量的稀H2SO4中,在标准状况下产生0.5mol气体,则混合物中所含的金属可能是( )
| A、Al和Mg |
| B、Al和Zn |
| C、Zn和Fe |
| D、Fe和Mg |
对相同质量的N2与NO作比较,正确的是( )
| A、所含的分子数相等 |
| B、在同温同压下,V(N2)═V(NO) |
| C、所含的原子数不相等 |
| D、在同温同体积下,p(N2)<p(NO) |
下列有关物质的性质或应用的说法正确的是( )
| A、石油裂化可获得乙烯、丙烯和丁二烯 |
| B、石油裂解的目的主要是为了得到更多的汽油 |
| C、盐析可用于提纯蛋白质并保持其生理活性 |
| D、木糖醇(C5H12O5)是一种甜味剂,它属于多羟基化合物,与葡萄糖互为同系物 |
一种新型熔融盐燃料电池具有高发电效率.现有Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2=2CO2.则下列说法中正确的是( )
| A、通CO的一极是正极 |
| B、负极发生的电极反应是:CO+CO32--2e-=2CO2 |
| C、正极发生氧化反应 |
| D、CO32-向正极定向移动 |
在水中水分子可彼此通过氢键形成(H2O)n的小集团.在一定温度下(H2O)n的n=5,每个水分子被4个水分子包围着形成四面体.(H2O)n的n=5时,下列说法中正确的是( )
| A、(H2O)n是一种新的水分子 |
| B、(H2O)n仍保留着水的化学性质 |
| C、1 mol(H2O)n中有2个氢键 |
| D、1 mol(H2O)n中有4 mol氢键 |
化学与工农业生产和人类生活密切相关.下列说法中错误的是( )
| A、晶体硅是良好的半导体材料,是信息技术的关键材料 |
| B、华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅 |
| C、硅胶常用于作干燥剂 |
| D、硅酸钠的水溶液俗称水玻璃,可用于制备木材防火剂 |
提出有机化学概念,使有机化学逐渐发展成为化学的一个重要分支的科学家是( )
| A、维勒 | B、贝采利乌斯 |
| C、李比希 | D、科里 |