题目内容
下列比较中,正确的是( )
| A、CH4与SiH4的稳定性:CH4>SiH4 |
| B、HClO与H2SO4的酸性:HClO>H2SO4 |
| C、1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和高 |
| D、Cl与S的原子半径:Cl>S |
考点:微粒半径大小的比较,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.非金属性越强,气态氢化物越稳定;
B.非金属性越强,最高价氧化物的水化物酸性越强,但HClO不是最高价氧化物的水化物;
C.燃烧为放热反应,则HCl分解为吸热反应;
D.同周期,原子序数大的原子半径小.
B.非金属性越强,最高价氧化物的水化物酸性越强,但HClO不是最高价氧化物的水化物;
C.燃烧为放热反应,则HCl分解为吸热反应;
D.同周期,原子序数大的原子半径小.
解答:
解:A.非金属性C>Si,气态氢化物稳定性为CH4>SiH4,故A正确;
B.非金属性越强,最高价氧化物的水化物酸性越强,但HClO不是最高价氧化物的水化物,HClO为弱酸,硫酸为强酸,酸性为HClO<H2SO4,故B错误;
C.燃烧为放热反应,则HCl分解为吸热反应,则1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和低,故C错误;
D.同周期,原子序数大的原子半径小,则Cl与S的原子半径为Cl<S,故D错误;
故选A.
B.非金属性越强,最高价氧化物的水化物酸性越强,但HClO不是最高价氧化物的水化物,HClO为弱酸,硫酸为强酸,酸性为HClO<H2SO4,故B错误;
C.燃烧为放热反应,则HCl分解为吸热反应,则1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和低,故C错误;
D.同周期,原子序数大的原子半径小,则Cl与S的原子半径为Cl<S,故D错误;
故选A.
点评:本题考查元素及化合物性质的比较,为高频考点,把握非金属性的比较方法、原子半径的比较方法及反应中的能量变化为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列关于金属冶炼说法正确的是( )
| A、工业上一般以铁矿石、焦炭、石灰石和空气等原料在高炉中冶炼生铁 |
| B、炼钢主要目的是在高温下用还原剂将过多的碳和其他杂质还原成气体或炉渣除去 |
| C、炼钢中添加硅、锰、铝等作为脱氧剂,调整钢水的成分,制成多种性能优良的钢材 |
| D、电解铝时阴极材料需要定期更换. |
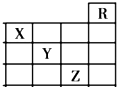 如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是( )①X的气态氢化物与Y最高价氧化物对应的水化物能发生反应生成盐
②等物质的量浓度的X、Y、Z的气态氢化物的水溶液的pH:X>Y>Z
③Z的单质常温下是液体,一定条件下可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素.
| A、只有③ | B、只有①④ |
| C、只有①②③④ | D、①②③④⑤ |
有机化合物A转化为B的反应如下,下列说法正确的是( )
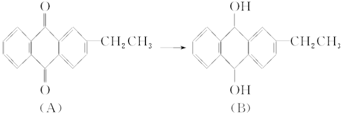

| A、B的分子式为C16H14O2 |
| B、上述转化属于还原反应 |
| C、二者均为芳香烃 |
| D、二者均能发生加成、酯化反应 |
X、Y、Z、W、R 5种短周期元素,其原子序数依次增大.X是元素周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A、Z与Y两种元素组成的化合物中,阴、阳离子个数比为1:1或1:2 |
| B、Y、Z、W元素形成的简单离子具有相同电子层结构,其离子半径依次增大 |
| C、Z、R元素的氧化物的水化物之间相互反应生成的盐溶液呈中性、碱性或酸性 |
| D、Y、R元素分别与X元素形成的化合物的沸点:XmY<XmR |
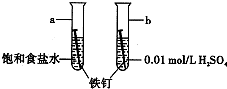 如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )
如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )| A、ab在两处的腐蚀速率a<b |
| B、a、b两处铁钉中的碳均为正极 |
| C、a、b两处铁钉中的铁均失电子被氧化 |
| D、a、b两处的正极反应式均为O2+4e-+4H+═2H2O |
下列说法正确的是( )
| A、有化学键断裂的过程一定发生化学变化 | ||
| B、氯化钠是一种电解质,电解饱和食盐水可制得金属钠 | ||
C、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| D、SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
化学与生产、生活、社会密切相关.下列说法中不正确的是( )
| A、“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B、绿色化学的核心是从源头上消除工业生产对环境的污染 |
| C、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| D、华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅 |