题目内容
5.某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、NO3-、Cl-、SO42-中的4种离子,所含离子均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).回答下列问题:①溶液中存在的离子是Na+、Fe2+、NO3-、SO42-;
②写出溶液中加入过量的稀硫酸反应的离子方程式3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
分析 ①向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变,则一定发生Fe2+、NO3-的氧化还原反应生成硝酸铁和NO,阴离子种类不变,则原溶液中存在SO42-,又溶液中含有四种离子,所含离子的物质的量均为1mol,由电荷守恒可知,含有带一个单位正电荷的阳离子,以此来解答;
②酸性溶液中Fe2+、NO3-的氧化还原反应生成硝酸铁和NO和水.
解答 解:①向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变,则一定发生Fe2+、NO3-的氧化还原反应生成硝酸铁和NO,阴离子种类不变,说明原溶液中原来已经存在SO42-,则不含Ba2+,又溶液中含有四种离子,反应生成了Fe3+,所含离子的物质的量均为1mol,由电荷守恒可知,含有带一个单位正电荷的阳离子,即一定含有Na+,由上述推断可知,该溶液中所含的离子为:Na+、Fe2+、NO3-、SO42-,
故答案为:Na+、Fe2+、NO3-、SO42-;
②向该溶液中加入过量的稀硫酸,稀硫酸中的氢离子和硝酸根离子将亚铁离子氧化为铁离子,同时会生成一氧化氮,发生反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
点评 本题考查以离子反应考查离子的推断,为高频考点,解答本题的关键是根据发生的有关化学反应确定存在的离子,注意掌握常见离子的性质及检验方法,题目难度中等.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
15.为除去镀在铝表面的铜层,且不会造成铝的损耗,可选用的试剂是( )
| A. | 浓硝酸 | B. | 稀硝酸 | C. | NaOH溶液 | D. | 浓盐酸 |
16.一定温度下,有两个体积均为2L的恒容密闭容器Ⅰ和Ⅱ,向Ⅰ中加入1molCO和2molH2,向Ⅱ中加入2molCO和4molH2,均发生下列反应,并建立平衡:CO(g)+2H2(g)?CH3OH(g).测得不同温度下CO平衡转化率如图所示.下列说法正确的是( )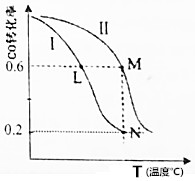

| A. | 该反应的△H>0 | |
| B. | M点化学平衡常数K=0.59 | |
| C. | L、M两点容器内压强:P(M)>2P(L) | |
| D. | 向N点平衡体系中再加入1molCH3OH,建立新平衡时被分解的CH3OH物质的量小于0.4mol |
20.有甲、乙两种溶液,甲溶液的pH是乙溶液pH的2倍,则甲溶液中c(H+)与乙溶液中c(H+)的关系是( )
| A. | 2:1 | B. | 100:1 | C. | 1:100 | D. | 无法确定 |
10.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 常温常压下,7.8克苯中含0.3NA个碳碳双键 | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
17.聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点.聚丙烯酸酯的结构简式为 它属于( )
它属于( )
①无机化合物 ②有机化合物 ③高分子化合物 ④小分子化合物 ⑤混合物 ⑥共价化合物.
 它属于( )
它属于( )①无机化合物 ②有机化合物 ③高分子化合物 ④小分子化合物 ⑤混合物 ⑥共价化合物.
| A. | ①③④ | B. | ①③⑤ | C. | ②③⑤⑥ | D. | ②③④ |
15.X、Y均为短周期元素,已知X+与Y2-具有相同的核外电子层结构.下列关于X和Y元素的性质推测正确的是( )
| A. | 原子半径X>Y | |
| B. | X与Y处于同一周期 | |
| C. | 离子半径X+>Y2- | |
| D. | X的单质与Y的单质发生反应只能生成X2Y |

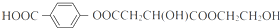 .
. .
.
 .
. .
.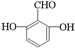 、
、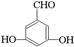 、
、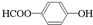 .
. A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题: