题目内容
25℃时,将0.2mol CH3COONa晶体和0.1mol HCl气体同时溶于蒸馏水,制得1L溶液.若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是( )
| A、该溶液的pH小于7 |
| B、c(CH3COOH)+c(CH3COO-)=0.20mol?L-1 |
| C、c(CH3COOH)<c(CH3COO-) |
| D、c(CH3COO-)+c(OH-)=0.10mol?L-1 |
考点:离子浓度大小的比较
专题:
分析:将0.2molCH3COONa晶体和0.1molHCl气体同时溶解于同一烧杯的水中,制得1L溶液,溶液中的溶质是醋酸钠和氯化钠、醋酸,且三者的物质的量浓度都是0.1mol/L,溶液中c(CH3COO-)>c(Cl-),则说明醋酸的电离程度大于醋酸根离子的水解程度,溶液显示酸性,据此进行判断.
解答:
解:A.溶液中的溶质是醋酸钠和氯化钠、醋酸,且三者的物质的量浓度都是0.1mol/L,溶液中c(CH3COO-)>c(Cl-),则说明醋酸的电离程度大于醋酸根离子的水解程度,则溶液呈酸性,即溶液的pH小于7,故A正确;
B.根据物料守恒得:c(CH3COOH)+c(CH3COO-)=0.20mol?L-1,故B正确;
C.醋酸的电离程度大于醋酸根离子的水解程度,所以c(CH3COOH)<c(CH3COO-),故C正确;
D.由电荷守恒可知c(CH3COO-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),c(Na+)=0.2mol/L,c(Cl-)0.1mol/L,则c(CH3COO-)+c(OH-)=0.2mol/L-0.1mol/L+c(H+)>0.10mol?L-1,c(CH3COO-)+c(OH-)>0.10mol?L-1,故D错误;
故选D.
B.根据物料守恒得:c(CH3COOH)+c(CH3COO-)=0.20mol?L-1,故B正确;
C.醋酸的电离程度大于醋酸根离子的水解程度,所以c(CH3COOH)<c(CH3COO-),故C正确;
D.由电荷守恒可知c(CH3COO-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),c(Na+)=0.2mol/L,c(Cl-)0.1mol/L,则c(CH3COO-)+c(OH-)=0.2mol/L-0.1mol/L+c(H+)>0.10mol?L-1,c(CH3COO-)+c(OH-)>0.10mol?L-1,故D错误;
故选D.
点评:本题考查离子浓度大小的比较,题目难度中等,明确溶液中的溶质及其醋酸的电离程度大于醋酸根离子的水解程度是解本题关键,利用电荷守恒和物料守恒进行分析解答.

练习册系列答案
相关题目
氯化银在水中存在沉淀溶解平衡,25℃时,氯化银的Ksp=1.8×10-10.现将足量氯化银分别放入:①100mL蒸馏水中;②100mL 0.1mol?L-1盐酸中;③100mL 0.1mol?L-1氯化铝溶液中,充分搅拌后,在相同温度下,c(Ag+)由大到小的顺序是( )
| A、①②③ | B、③②① |
| C、②①③ | D、②③① |
在一定条件下,同一物质中不能自身相互发生反应的是( )
| A、乙醇 | B、氨基酸 |
| C、乙烯 | D、硬脂酸 |
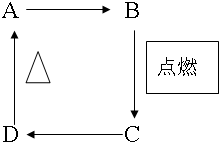 中学化学中常见化合物A、B、C、D的转化关系如图(某些反应物、产物略去).常温下B、C都是气体,又知A、C都是酸性氧化物,其中A是一种高熔点化合物,不溶于硫酸、硝酸、却溶于氢氟酸,固体C可用于人工降雨
中学化学中常见化合物A、B、C、D的转化关系如图(某些反应物、产物略去).常温下B、C都是气体,又知A、C都是酸性氧化物,其中A是一种高熔点化合物,不溶于硫酸、硝酸、却溶于氢氟酸,固体C可用于人工降雨
 的所有原子
的所有原子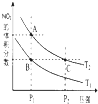 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.