题目内容
当溶液中的Fe2+和〔RO(OH)2〕+粒子数之比为2:1时正好完全发生氧化还原反应(Fe2+转变为Fe3+),则R元素在产物中的价态为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
考点:氧化还原反应的计算
专题:计算题
分析:根据氧化还原反应中,化合价升高值=化合价降低值=转移电子数,根据电子守恒进行计算即可.
解答:
解:RO(OH)2〕+中R的化合价是+5价,设R元素在产物中的价态为x,则2×(3-2)=1×(5-x),解得x=3.
故选B.
故选B.
点评:本题考查学生电子守恒的计算知识,注意知识的归纳和梳理是关键,难度不大.

练习册系列答案
 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
下列有关反应热的说法中正确的是( )
A、己知C(s)+O2(g)=CO2(g);△H1C(s)+
| ||
| B、中和热△H=-57.3kJ?mol-1,所以1.00L 1.00mol?L-1H2SO4与稀的NaOH溶液恰好完全反应放出57.3kJ的热量 | ||
| C、用等体积的0.50mol?L-1盐酸、0.55mol?L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大 | ||
| D、在101KPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
下列变化需加入还原剂才能实现的是( )
| A、HCl→Cl2 | ||
| B、Fe→Fe3+ | ||
| C、KClO3→O2 | ||
D、MnO
|
下列事实与胶体性质无关的是( )
| A、水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 |
| B、一束平行光线射入氢氧化铁胶体里,从侧面可以看到一条光亮的通路 |
| C、将植物油倒入水中用力搅拌形成油水混合物 |
| D、氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 |
 乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,②键和⑤断裂 |
| C、在铜催化下和氧气反应时,键①和③断裂 |
| D、与氢卤酸反应时,①键断裂 |
一定条件下,在反应:2SO2(g)+O2(g)?2SO3(g)的化学平衡体系中,SO2、O2、SO3的浓度分别为2mol?L-1、0.8mol?L-1、2.4mol?L-1,则O2在反应起始时可能的浓度范围是( )
| A、0.8~2.0 mol?L-1 |
| B、0~2.0 mol?L-1 |
| C、0~0.8 mol?L-1 |
| D、无法确定 |
如图所示,关于该装置的下列叙述中,不正确的是( )
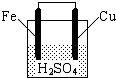

| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、电流从锌片经导线流向铜片 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
下列关于摩尔质量的叙述正确的是( )
| A、1molH2SO4的质量是98g/mol |
| B、CO2的摩尔质量等于CO2的相对分子质量 |
| C、1mol任何物质的质量等于该物质的相对分子质量 |
| D、Na的摩尔质量是23g/mol |
下列有关说法正确的是( )
| A、放热反应在任何条件都能自发进行 |
| B、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C、任何能使熵值增大的过程都能自发进行 |
| D、△H>0,△S<0的化学反应一定能自发进行 |