题目内容
已建立化学平衡的某可逆反应,改变条件使化学平衡向正反应方向移动,下列有关叙述正确的是( )
| A、此时正反应速率一定大于逆反应速率 |
| B、反应一定放出热量 |
| C、平衡时反应物的浓度一定降低 |
| D、平衡时生成物的质量分数一定增加 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:影响化学平衡状态的因素有浓度、温度、压强等,外界条件不同,对平衡移动的影响不同,改变条件使化学平衡向正反应方向移动,则正反应速率一定大于逆反应速率,据此分析.
解答:
解:A、正反应速率大于逆反应速率,平衡向正反应方向移动,故A正确;
B、给吸热反应升温时,平衡正向移动,故B错误;
C、减小容器体积导致平衡移动时,各物质浓度都增大,故C错误;
D、减小生成物浓度使平衡正向移动时,该生成物质量分数降低,故D错误;
故选A.
B、给吸热反应升温时,平衡正向移动,故B错误;
C、减小容器体积导致平衡移动时,各物质浓度都增大,故C错误;
D、减小生成物浓度使平衡正向移动时,该生成物质量分数降低,故D错误;
故选A.
点评:本题考查化学平衡的影响因素,题目难度中等,注意影响化学平衡移动的三因素,解答时注意从勒沙特列原理的角度分析.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、饱和氯水中 Cl-、NO3-、Na+、SO32- |
| B、强酸性的溶液中 C6H5O-、K+、SO42-、Br- |
| C、Na2S溶液中 SO42-、K+、Cl-、Cu2+ |
| D、强碱性的溶液中 NO3-、I-、Na+、AlO2- |
下列物质是电解质的为( )
| A、氨气 | B、硫酸钡 |
| C、水玻璃 | D、硝酸钾溶液 |
在一定条件下,对于密闭容器中进行的可逆反应:2HI(g)?H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
| A、HI、H2、I2的浓度不再发生变化 |
| B、HI、H2、I2的浓度相等 |
| C、HI、H2、I2在密闭容器中共存 |
| D、反应停止,正、逆反应速率都等于零 |
用于飞机制造的重要材料是( )
| A、Mg-Al合金 |
| B、Cu-Sn合金 |
| C、Fe-Si合金 |
| D、不锈钢 |
硅及其化合物在材料领域中应用广泛.下列叙述错误的是( )
| A、光导纤维的主要成分是二氧化硅 |
| B、硅酸不溶于水,且硅酸的酸性比碳酸弱 |
| C、不用带玻璃瓶塞的试剂瓶盛放NaOH溶液 |
| D、二氧化硅不溶于水,也不溶于任何酸 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、c(H+)=1.0×10-13mol/L溶液中:CH3COO-、K+、SO42-、Br- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D、pH=12的溶液中:NO3-、I-、Na+、Al3+ |
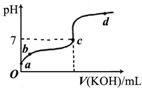 已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题:
已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题: