题目内容
19.用CH4催化还原NOX可以消除氮氧化物的污染.例如:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
已知NO、NO2混合气体的密度是相同条件下氢气密度的17倍,16g甲烷和该混合气体恰好完全反应生成N2、CO2、H2O(g)放出1042.8kJ的热量,则△H1是( )
| A. | -867kJ•mol-1 | B. | -574kJ•mol-1 | C. | -691.2kJ•mol-1 | D. | -925.6kJ•mol-1 |
分析 NO、NO2混合气体的密度是相同条件下氢气密度的17倍,则混合气体的平均相对分子质量=17×2=34,设NO的物质的量分数为x,则NO2的物质的量分数为1-x,
30x+46(1-x)=34 x=0.75 则混合气体中NO、NO2的物质的量之比为:0.75:0.25=3:1,16g甲烷的物质的量为n=$\frac{m}{M}$=$\frac{16g}{16g/mol}$=1mol,则与16g甲烷反应的物质的量分别为0.75mol、0.25mol,结合放出1042.8kJ的热量进行计算.
解答 解:NO、NO2混合气体的密度是相同条件下氢气密度的17倍,则混合气体的平均相对分子质量=17×2=34,设NO的物质的量分数为x,则NO2的物质的量分数为1-x,
30x+46(1-x)=34 x=0.75 则混合气体中NO、NO2的物质的量之比为:0.75:0.25=3:1,16g甲烷的物质的量为n=$\frac{m}{M}$=$\frac{16g}{16g/mol}$=1mol,则与16g甲烷反应的物质的量分别为0.75mol、0.25mol,16g甲烷和该混合气完全反应生成N2、CO2、H2O(g)放出1042.8kJ的热量,则1160KJ/mol×0.75mol+△H 1×0.25mol=1042.8KJ,+△H 1=-691.2KJ/mol,
故选C.
点评 本题考查混合物的计算和反应热的计算,侧重于学生的分析、计算能力的考查,注意把握计算的思路,注意理解运用.题目难度中等.

练习册系列答案
相关题目
10.N、O、Si、S、Al、Fe、Cu是常见的七种元素.
(1)Si位于元素周期表第三周期第IVA族.
(2)Cu原子的价层电子排布图为 .
.
(3)基态Fe原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5.可用硫氰化钾检验Fe3+,形成的配合物的颜色为血红色.
(4)用“>”或“<”填空:
(5)氢元素和上述非元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为sp3;分子中既含有极性共价键、又含有非极性共价键的化合物是H2O2 或N2H4(填化学式,任写一种).
(6)O和Cu形成的一种离子化合物的晶体结构如图,则铜离子的电荷为+1.
(1)Si位于元素周期表第三周期第IVA族.
(2)Cu原子的价层电子排布图为
 .
.(3)基态Fe原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5.可用硫氰化钾检验Fe3+,形成的配合物的颜色为血红色.
(4)用“>”或“<”填空:
| 离子半径 | 电负性 | 熔点 | 酸性 |
| O2-> Na+ | F>O | 金刚石> 晶体硅 | H2SO4<HClO4 |
(6)O和Cu形成的一种离子化合物的晶体结构如图,则铜离子的电荷为+1.

7.下列叙述错误的是( )
(1)石油裂解、煤的气化、溶液导电都属于化学变化
(2)H2S水溶液是弱酸,HCl水溶液是强酸,可以验证硫元素的非金属性比氯元素弱
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物.
(1)石油裂解、煤的气化、溶液导电都属于化学变化
(2)H2S水溶液是弱酸,HCl水溶液是强酸,可以验证硫元素的非金属性比氯元素弱
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物.
| A. | 全部 | B. | (2)(3)(4) | C. | (1)(2)(3)(5) | D. | (2)(3)(4)(5) |
14.下列分子中的所有原子一定在同一平面上的是( )
| A. | 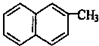 | B. | 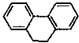 | C. | 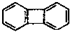 | D. | 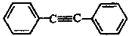 |
11.下列有机物在空气中燃烧的说法正确的是( )
| A. | 只有碳的氧化物和水 | |
| B. | 只有CO2和水 | |
| C. | 可能有碳的氧化物、水及其他元素的化合物 | |
| D. | 有CO、CO2、水及其他元素的化合物 |
 有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如图转化:已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为
有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如图转化:已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为 (其中:-X、-Y均为官能团).
(其中:-X、-Y均为官能团). .
. .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.