题目内容
17.含硫的物质与人们的生活密切相关.已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化.完成下列填空:(1)写出浓硫酸与铜共热反应的化学方程式Cu+2H2SO4(浓) $\frac{\underline{\;加热\;}}{\;}$CuSO4+2H2O+SO2↑.
(2)250C,1atm下,1克硫粉在氧气中充分燃烧放出 9.36kJ热量,写出硫燃烧的热化学方程式S(s)+O2(g)═SO2(g),△H=-299.52kJ/mol.
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸.
你认为减少酸雨产生的途径可采用的措施是C.
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③B.②③④⑤C.①③⑤D.①③④⑤
分析 (1)铜与浓硫酸在加热条件下生成二氧化硫、硫酸铜和水,据此书写方程式;
(2)热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比;
(3)二氧化硫与水反应生成亚硫酸,易被氧化为硫酸,雨水酸性增强;少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成.把工厂烟囱造高、在已酸化的土壤中加石灰等措施不能有效地防止酸雨的形成.
解答 解:(1)铜与浓硫酸在加热条件下生成二氧化硫、硫酸铜和水,方程式:Cu+2H2SO4(浓) $\frac{\underline{\;加热\;}}{\;}$CuSO4+2H2O+SO2↑;
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;加热\;}}{\;}$CuSO4+2H2O+SO2↑;
(2)1g硫粉完全燃烧生成二氧化硫气体,放出9.36kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出299.52kJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g),△H=-290.52kJ/mol,
故答案为:S(s)+O2(g)═SO2(g),△H=-299.52kJ/mol;
(3)二氧化硫与水反应生成亚硫酸,易被氧化为硫酸,雨水酸性增强,则由二氧化硫形成的酸雨的主要成分是硫酸(H2SO4),把工厂烟囱造高、在已酸化的土壤中加石灰等措施不能从源头有效地防止酸雨的形成,少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成,故答案为:硫酸(H2SO4);C.
点评 本题主要考查浓硫酸的性质和酸雨的形成,掌握二氧化硫的性质生成途径和处理方法是解答的关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I 是一种白色晶体,下 列对 PH4I 的叙述中,正确的是( )
| A. | 它是一种共价化合物 | B. | 它受热时,不能分解产生有色气体 | ||
| C. | 它不可能与 NaOH 溶液反应 | D. | 它既含离子键又含共价键 |
5.1mol硫酸铁与1mol铁恰好完全反应,则产物的物质的量为( )
| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
12.关于铝及其化合物的说法错误的是( )
| A. | 氧化铝是一种高硬度高熔沸点化合物 | |
| B. | 铝是活泼金属,其合金抗腐蚀能力差 | |
| C. | 常温下铝能与氧气反应 | |
| D. | 氢氧化铝能中和胃酸,可用于制胃药 |
6.CH2=CH2与CH2=CR2(R为烃基)的混合物在一定条件下发生加聚反应,生成的产物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.X、Y、Z、M、N、q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是( )
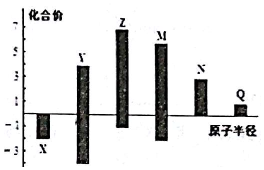

| A. | 金属性:N>Q | |
| B. | 最高价氧化物对应水化物酸性:M>Y>N | |
| C. | 简单离子半径:Q>N>X | |
| D. | 原子序数:Z>M>X>Y |
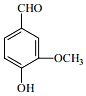 香荚兰豆的香气成分中含有的香草醛(如图)也称香兰素,常用做食品添加剂的原料,起着增香作用.请回答下列问题:
香荚兰豆的香气成分中含有的香草醛(如图)也称香兰素,常用做食品添加剂的原料,起着增香作用.请回答下列问题: