题目内容
19.通过以下反应可获得新型能源二甲醚(CH3OCH3 ).下列说法不正确的是( )①C(s)+H2O(g)═CO(g)+H2 (g)△H1=a kJ•mol-1
②CO(g)+H2O(g)═CO2 (g)+H2 (g)△H 2=b kJ•mol-1
③CO2(g)+3H2 (g)═CH3OH(g)+H2O(g)△H3=c kJ•mol-1
④2CH3OH(g)═CH3OCH3 (g)+H2O(g)△H 4=d kJ•mol-1.
| A. | 反应③的原料是由反应①、②提供的 | |
| B. | 反应③可以作为解决温室效应方案之一 | |
| C. | 反应CH3OH(g)═CO (g)+2H2(g)的△H=(-b-c)kJ•mol-1 | |
| D. | 反应 2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(l)的△H=( 2b+2c+d ) kJ•mol-1 |
分析 A.反应③中的反应物为CO2、H2;
B.反应③中的反应物为CO2,可减少二氧化碳的含量;
C.由盖斯定律可知将(②+③)×(-1)得到CO2(g)+3H2 (g)═CH3OH(g)+H2O(g);
D.由盖斯定律可知,②×2+③×2+④得到2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g).
解答 解:A.反应③中的反应物为CO2、H2,由反应可知,反应①、②为反应③提供原料气,故A正确;
B.反应③中的反应物为CO2,转化为甲醇,可以作为解决温室效应方案之一,故B正确;
C.由盖斯定律可知将(②+③)×(-1)得到CO2(g)+3H2 (g)═CH3OH(g)+H2O(g)△H=(-b-c)kJ•mol-1,故C正确;
D.由盖斯定律可知,②×2+③×2+④得到2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g),则△H=( 2b+2c+d ) kJ•mol-1,水的状态不同,故D错误.
故选D.
点评 本题考查反应热与焓变,为高频考点,把握反应的特点、反应中能量变化、盖斯定律应用为解答的关键,侧重分析能力和应用能力的考查,题目难度中等.

练习册系列答案
相关题目
5.下列图示与对应的叙述相符的是( )

| A. | 图1表示可以判断:若T1>T2,反应A(g)+B(g)?2C(g)△H<0 | |
| B. | 图2表示0.1000mol•L-1CH3COOH溶液滴定20.00mL0.1000mol•L-1NaOH溶液所得到的滴定曲线 | |
| C. | 图3表示压强对可逆反应2A(g)+2B(g)?3C(g)+Ds(g)的影响,甲比乙的压强大 | |
| D. | 如图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在6.5左右 |
7.下列实验方案能达到实验目的是( )
| A. | 用苯和饱和溴水制溴苯 | |
| B. |  用图所示装置制备乙酸乙酯 | |
| C. | 常温下苯酚的溶解度很小,可以过滤分离水中未完全溶解的苯酚 | |
| D. | 在溴乙烷水解混合体系中滴加硝酸银溶液检验溴离子的存在 |
14.下列关于碱金属及其化合物的说法不正确的是( )
| A. | 从锂到铯与水反应越来越剧烈 | B. | 液态钠可用作核反应堆的传热介质 | ||
| C. | Li在氧气中燃烧生成Li2O2 | D. | 氢氧化铯的碱性强于氢氧化钠 |
11.下列关于电解质溶液的叙述正确的是( )
| A. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| B. | 常温下,饱和氯水中c(H+)-c(OH-)═c(Cl-)+C(ClO-) | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
8.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的有机物,下列说法中正确的是( )
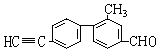

| A. | 分子中处于同一直线上的碳原子最多有7个 | |
| B. | 分子中至少有16个碳原子处于同一平面上 | |
| C. | 该有机物可发生加成反应和消去反应 | |
| D. | 该有机物分子式C16H10O |
12.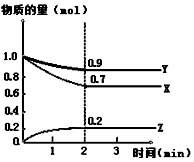 某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
 某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )| A. | 用X表示该化学反应速率比用Y表示的要快 | |
| B. | 该反应的化学方程式:3X+Y?2Z | |
| C. | 若在3min后,把Z从反应体系中分离,平衡不移动 | |
| D. | 反应开始至2min,Z的平均反应速率:0.1mol/(L•min) |