题目内容
氯化铁溶液和氢氧化铁胶体共同具有的性质是( )
| A、分散质微粒都能透过滤纸 |
| B、都有丁达尔现象 |
| C、加入盐酸后,都先产生沉淀,然后沉淀又溶解 |
| D、都有电泳现象 |
考点:胶体的重要性质
专题:
分析:A、胶体粒子直径比溶液大,比浊液小,胶体能透过滤纸;
B、胶体具有丁达尔效应;
C、氯化铁中加入盐酸无现象;
D、胶体具有电泳现象.
B、胶体具有丁达尔效应;
C、氯化铁中加入盐酸无现象;
D、胶体具有电泳现象.
解答:
解:A、胶体和溶液均能通过滤纸,故A正确;
B、胶体具有丁达尔效应,溶液不具备,故B错误;
C、氯化铁中加入盐酸无现象,故C错误;
D、胶体粒子表面积较大,能吸附电荷而带电,具有电泳现象,溶液不具备,故D错误,故选A.
B、胶体具有丁达尔效应,溶液不具备,故B错误;
C、氯化铁中加入盐酸无现象,故C错误;
D、胶体粒子表面积较大,能吸附电荷而带电,具有电泳现象,溶液不具备,故D错误,故选A.
点评:本题考查胶体的性质,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为( )
| A、11:1 | B、9:1 |
| C、1:11 | D、1:9 |
下列物品所用材料是SiO2的是( )
| A、普通玻璃餐具 |
| B、计算机芯片 |
| C、硅太阳能电池 |
| D、水晶镜片 |
对下列事实的解释,反应的离子方程式正确的是( )
| A、氢硫酸是一种二元弱酸:H2S?S2-+2H+ |
| B、工业用FeCl3溶液腐蚀铜线铝板:2Fe3-+Cu?2Fe2++Cu2+ |
| C、Al溶于NaOH溶液:2Al+2OH-=2AlO2-+H2↑ |
| D、用食醋除去水壶中的水后:2H++CaCO3=Ca2-+H2O+CO2 |
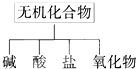 无机化合物可根据其组成和性质进行分类:
无机化合物可根据其组成和性质进行分类: 有X、Y、Z 3种元素,X是有机化合物中必含的元素,Y是地壳里含量最多的元素,Z是质量最轻的元素.X与Y能结合成两种化合物A和B,A可以燃烧,B不可以燃烧,也不支持燃烧;X与Z结合的最简单的化合物C有可燃性;X、Y与Z三种元素结合的化合物D常用做实验室加热的燃料.
有X、Y、Z 3种元素,X是有机化合物中必含的元素,Y是地壳里含量最多的元素,Z是质量最轻的元素.X与Y能结合成两种化合物A和B,A可以燃烧,B不可以燃烧,也不支持燃烧;X与Z结合的最简单的化合物C有可燃性;X、Y与Z三种元素结合的化合物D常用做实验室加热的燃料.
 在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应达到平衡后,测得混合气体为7体积.
在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应达到平衡后,测得混合气体为7体积.