题目内容
7.铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.①Cu位于元素周期表第ⅠB族.Cu2+的核外电子排布式为[Ar]3d9或1s22s22p63s23p63d9.
②Cu2O的熔点比Cu2S的高(填“高”或“低”),请解释原因氧离子半径比硫离子半径小,Cu2O比Cu2S的离子键强,所以Cu2O熔点高.
分析 ①Cu位于元素周期表第ⅠB族原子序数为29,根据Cu的电子排布式书写Cu2+离子的电子排布式;
②Cu2O与Cu2S都为离子晶体,离子半径越小,离子键越强,对应的熔点越高.
解答 解:①Cu(电子排布式为:[Ar]3d104s1)Cu2+的过程中,参与反应的电子是最外层的4s及3d上各一个电子,故Cu2+离子的电子排布式是为:[Ar]3d9或1s22s22p63s23p63d9,故答案为:[Ar]3d9或1s22s22p63s23p63d9;
②Cu2O与Cu2S都为离子晶体,离子半径越小,离子键越强,对应的熔点越高,因氧离子半径比硫离子半径小,Cu2O比Cu2S的离子键强,所以Cu2O熔点高.
故答案为:高;氧离子半径比硫离子半径小,Cu2O比Cu2S的离子键强,所以Cu2O熔点高.
点评 本题考查常见元素核外电子排布、离子键以及晶格能等知识,为高频考点,题目难度中等,学习中注意加强对核外电子排布的学习.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
15.下列有关环境问题的说法不正确的是( )
| A. | 燃煤时加入适量石灰石,可减少废气中SO2的含量 | |
| B. | 京津冀、长三角、珠三角雾霾的形成与煤的燃烧、化工厂大量排放含硫、含氮氧化物、颗粒物和汽车排放的尾气等有关 | |
| C. | pH小于7.0的降雨通常称为酸雨 | |
| D. | 使用洁净能源、为汽车安装尾气转化装置、对硝酸厂排放的废气进行碱处理能有效控制氮氧化物对空气的污染 |
2.“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是( )
| A. | 构造原理 | B. | 泡利不相容原理 | C. | 洪特规则 | D. | 能量最低原理 |
19.下列有关化学药品的保存和运输不正确的是( )
| A. | 浓硝酸应保存在棕色试剂瓶并置于阴凉处 | |
| B. | 氢氟酸不能装在玻璃瓶,应装在塑料瓶中 | |
| C. | NaOH溶液用带磨口玻璃瓶塞的试剂瓶保存 | |
| D. | 常温下浓硫酸和浓硝酸可以铁制槽罐车运输 |
16.向100ml 18mol/L硫酸溶液中加入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量是( )
| A. | 小于0.9mol | B. | 等于0.9mol | ||
| C. | 在0.45mol与0.9mol之间 | D. | 大于0.9mol |
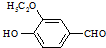 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.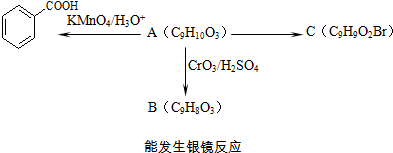
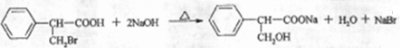
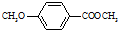 )是一种医药中间体.
)是一种医药中间体. )合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.
)合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.