题目内容
7.表为元素周期表中短周期的一部分,其中Y元素的原子序数等于M与N元素原子序数之和.下列说法错误的是( )| M | N | ||
| X | Y | Z |
| A. | 最简单氢化物的稳定性:M>N>Z | B. | 最高价含氧酸的酸性:Z>M>Y | ||
| C. | 单质的熔点:X>Z>N | D. | 简单离子的半径:Z>N>X |
分析 M、Y在同一主族,Y元素的原子序数为M与N元素原子序数之和,可知N的原子序数为8,由原子在周期表中的相对位置可知X为Al、M为C,Y为Si,Z为S元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:由以上分析可知X为Al、M为C、Y为Si、N为O元素、Z为S元素,
A.非金属性O>S>C,元素的非金属性越强,对应的氢化物越稳定,故A错误;
B.非金属性S>C>Si,元素的非金属性越强,对应的最高价含氧酸的酸性越强,故B正确;
C.Al为金属晶体,熔点最高,S常温下为固体,氧气为气体,则单质的熔点:X>Z>N,故C正确;
D.一般来说,核外电子层数越多,离子半径越大,具有相同的核外电子排布,核电荷数越大,离子半径越小,则简单离子的半径:Z>N>X,故D正确.
故选A.
点评 本题考查位置、结构与性质的应用,为高频考点,把握元素的位置、元素化合物知识推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
17.醋酸镍[(CH3COO)2Ni]是一种重要的化工原料.一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料制取醋酸镍的工艺流程图如图1:

相关离子生成氢氧化物的pH和相关物质的溶解性如表:
(1)NH4F的电子式为
(2)将含镍原料粉碎的目的是提高镍的浸出率
(3)调节pH步骤中,溶液pH的调节范围是5.0≤pH<6.7.
(4)滤渣1和滤渣3主要成分的化学式分别是SiO2、CaSO4、CaF2.
(5)写出氧化步骤中加入H2O2发生反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(6)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体.写出该反应的化学方程式:NiS+H2SO4+2HNO3═NiSO4+SO2↑+2NO↑+2H2O.
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图2.酸浸的最佳温度与时间分别为70℃、120min.
(8)沉镍过程中,若c(Ni2+)=2.0mol•L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol•L-1],则需要加入Na2CO3固体的质量最少为31.8g.(保留小数点后1位有效数字).

相关离子生成氢氧化物的pH和相关物质的溶解性如表:
| 金属离子 | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
| 物质 | 20℃时溶解性(H2O) |
| CaSO4 | 微溶 |
| NiF | 可溶 |
| CaF | 难溶 |
| NiCO3 | Ksp=1.0×10-6 |

(2)将含镍原料粉碎的目的是提高镍的浸出率
(3)调节pH步骤中,溶液pH的调节范围是5.0≤pH<6.7.
(4)滤渣1和滤渣3主要成分的化学式分别是SiO2、CaSO4、CaF2.
(5)写出氧化步骤中加入H2O2发生反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(6)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体.写出该反应的化学方程式:NiS+H2SO4+2HNO3═NiSO4+SO2↑+2NO↑+2H2O.
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图2.酸浸的最佳温度与时间分别为70℃、120min.
(8)沉镍过程中,若c(Ni2+)=2.0mol•L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol•L-1],则需要加入Na2CO3固体的质量最少为31.8g.(保留小数点后1位有效数字).
18.巨噬细胞控制肌肉再生的“分子开关”的结构如图所示.下列有关说法错误的是( )
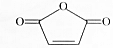

| A. | 分子式为C4H2O3 | B. | 能发生水解反应 | ||
| C. | 一氯代物有2种 | D. | 能使酸性KMnO4溶液褪色 |
15.在密闭容器中,反应2X(g)+Y(g)?3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是( )
| A. | v(正)减小,v(逆)增大 | B. | v(正)增大,v(逆)减小 | C. | v(正)、v(逆)都减小 | D. | v(正)、v(逆)都增大 |
2.用CH4还原NO2可以消除氮的氧化物对环境的污染,热化学方程式如下:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=-867.0KJ•mol-1下列说法错误的是( )
| A. | CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(l)△H<-867.0 KJ•mol-1 | |
| B. | 若增加甲烷的用量,平衡后体系中CO2的百分含量不一定升高 | |
| C. | 使用催化剂,可以降低反应的活化能,减少反应所放出的热量 | |
| D. | 标准状况下4.48 L CH4参加反应,转移电子数为1.6 NA |
12.甲、乙、丙三种物质是某抗生素合成过程中的中间产物,下列说法正确的是( )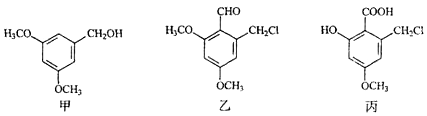

| A. | 甲、乙均能发生加成反应 | |
| B. | 甲的一种同分异构体中可能含有苯环和羧基 | |
| C. | 甲分子中的所有原子可能共平面 | |
| D. | 用酸性KMnO4溶液可鉴别乙和丙 |
19.下列与化学有关的说法中错误的是( )
| A. | 候氏制碱、制取肥皂的工艺过程中均应用了物质溶解度的差异 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定过程中利用了焰色反应 | |
| D. | 使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 |
6.已知碘在四氯化碳液体中的溶解度远大于在水中的溶解度,且固体碘在受热时,易直接变成气体,欲把碘从饱和碘水中分离出来,可采用的方法和主要仪器为( )
| A. | 蒸发、结晶与蒸发皿 | B. | 过滤与漏斗 | ||
| C. | 萃取、分液与分液漏斗 | D. | 蒸馏与蒸馏装置 |
7.要检验某溴乙烷中的溴元素,正确的实验方法是( )
| A. | 加入氯水振荡,观察水层是否有红棕色出现 | |
| B. | 滴入 AgNO3溶液,再加入稀 HNO3,观察有无浅黄色沉淀生成 | |
| C. | 加入 NaOH 溶液共热,然后加入稀 HNO3使溶液呈酸性,再滴入 AgNO3溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入 NaOH 溶液共热,冷却后加入 AgNO3溶液,观察有无浅黄色沉淀生成 |