题目内容
1.下列分子中,所有原子的最外层均为8电子稳定结构的是( )| A. | BeCl2 | B. | H2S | C. | PCl3 | D. | SF4 |
分析 对于共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,以此解答该题.
解答 解:A.BeCl2中Be元素的化合价是+2价,其最外层有2个电子,所以化合价的绝对值与其最外层电子数之和是4,故A错误;
B.硫化氢中氢原子最外层有1个电子,其化合价是+1价,所以不能满足最外层8电子结构,故B错误;
C.PCl3中氮原子最外层电子数=5+3=8,氯原子最外层电子数=7+|-1|=8,所以所有原子都满足最外层8电子结构,故C正确;
D.SF4中硫原子最外层电子数=4+6=10,所以S原子不满足8电子结构,故D错误;
故选C.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
相关题目
1.在反应2F2+2H2O═4HF+O2中,H2O是( )
| A. | 氧化剂 | B. | 还原剂 | C. | 溶剂 | D. | 催化剂 |
12.下列说法中正确的是( )
| A. | 二氧化硫可广泛用于食品的增白 | |
| B. | 用硫酸清洗锅垢中的水垢 | |
| C. | 用SO2漂白纸浆和草帽辫 | |
| D. | 因为浓硫酸有强氧化性,故浓硫酸可用于干燥H2和CO |
9.在使酚酞变红的溶液中,能大量共存的离子组是( )
| A. | Na+ HCO3- SO42- Br- | B. | Cu2+ K+ SO42- NO3- | ||
| C. | Na+ K+ Cl- NO3- | D. | Fe3+ K+ SO42- Cl- |
16. 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(2)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填字母序号,下同).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-)
D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E. $\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$
若该溶液升高温度,上述5种表达式的数据增大的是ABCE.
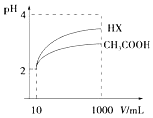
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是HX酸性强于CH3COOH的,稀释后HX溶液中的c(H+)小于CH3COOH溶液中的c(H+),所以其对水电离的抑制能力也较弱.
(4)已知100℃时,水的离子积为1×10-12,该温度下测得某溶液pH=7,该溶液显碱(填“酸”、“碱”或“中”)性.将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=11:9.
 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5mol•L-1 | K1=4.4×10-7mol•L-1 K2=5.6×10-11mol•L-1 | 3.0×10-8 mol•L-1 |
(1)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(2)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填字母序号,下同).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-)
D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E. $\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$
若该溶液升高温度,上述5种表达式的数据增大的是ABCE.
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是HX酸性强于CH3COOH的,稀释后HX溶液中的c(H+)小于CH3COOH溶液中的c(H+),所以其对水电离的抑制能力也较弱.
(4)已知100℃时,水的离子积为1×10-12,该温度下测得某溶液pH=7,该溶液显碱(填“酸”、“碱”或“中”)性.将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=11:9.
13.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-Q1KJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-$\frac{1}{2}$Q2•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-$\frac{1}{2}$Q3•mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量(单位:KJ)为( )
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-$\frac{1}{2}$Q2•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-$\frac{1}{2}$Q3•mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量(单位:KJ)为( )
| A. | 0.4Q1+0.05Q3 | B. | 0.4Q1+0.05Q2 | C. | 0.4Q1+0.1Q3 | D. | 0.4Q1+0.2Q2 |
10.下列化合物的核磁共振氢谱中出现三个峰的是( )
| A. | 2,5-二甲基己烷 | B. | 2,2-二甲基丙烷 | ||
| C. | 2,6-二甲基庚烷 | D. | 2,2,3,3-四甲基丁烷 |
