题目内容
向200mL 0.5mol?L-1H2SO4溶液中投入足量的锌,充分反应.计算:
(1)标准状况下生成H2的体积.
(2)所得溶液溶质物质的量浓度.(假定反应前后溶液体积不不发生变化) .
(1)标准状况下生成H2的体积.
(2)所得溶液溶质物质的量浓度.(假定反应前后溶液体积不不发生变化)
考点:化学方程式的有关计算
专题:计算题
分析:发生反应Zn+H2SO4=ZnSO4+H2↑,Zn足量,硫酸完全反应,根据n=cV计算H2SO4的物质的量,根据方程式计算生成H2、ZnSO4的物质的量,根据V=nVm计算氢气体积,根据c=
计算ZnSO4的物质的量浓度.
| n |
| V |
解答:
解:200mL 0.5mol?L-1H2SO4溶液中H2SO4的物质的量=0.2L×0.5mol/L=0.1mol,则:
Zn+H2SO4=ZnSO4+H2↑
0.1mol 0.1mol 0.1mol
(1)标况下,生成氢气的体积=0.1mol×22.4L/mol=2.24L,
故答案为:2.24L;
(2)ZnSO4的物质的量浓度=
=0.5mol/L,
故答案为:0.5mol/L.
Zn+H2SO4=ZnSO4+H2↑
0.1mol 0.1mol 0.1mol
(1)标况下,生成氢气的体积=0.1mol×22.4L/mol=2.24L,
故答案为:2.24L;
(2)ZnSO4的物质的量浓度=
| 0.1mol |
| 0.2L |
故答案为:0.5mol/L.
点评:本题考查化学方程式的有关计算,比较基础,(2)中利用硫酸根守恒计算更简单.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、Al2(SO4)3可除去酸性废水中的悬浮颗粒 |
| B、氯气与石灰乳反应能得到含氯漂白剂 |
| C、燃煤时加入适量石灰石,可减少废气中SO2的排放 |
| D、工业上硝酸可用于制化肥、农药、炸药和染料等 |
将13.5g金属铝与1L 2mol?L-1的NaOH溶液充分反应,生成的气体在标准状况下的体积为( )
| A、11.2 L |
| B、16.8 L |
| C、33.6 L |
| D、44.8 L |
下列反应中,属于吸热反应的是( )
| A、木炭在空气中燃烧 |
| B、氢气在氯气中燃烧 |
| C、盐酸和氢氧化钠溶液反应 |
| D、将Ba(OH)2?8H2O晶体和NH4C1晶体研细后混合并搅拌 |
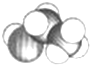 乙醇是生活中常见的一种有机物,它的分子结构模型如图所示:
乙醇是生活中常见的一种有机物,它的分子结构模型如图所示: