题目内容
19.在标准状况下,将7.84LH2S和11.2LO2混合放入一密闭容器中,点燃,使之反应.恢复到原状态,经测定反应物均无剩余,则反应后的氧化产物的总质量为21.6克.分析 反应后的氧化物中含有硫元素,氧化产物为硫或二氧化硫或SO2、S,同时生成水,反应物均无剩余,由质量守恒可知,混合气体的总质量减去生成的水的质量为容器中氧化产物的质量,由元素守恒可知n(H2O)=n(H2S),根据m=nM计算m(H2O),据此解答.
解答 解:标准状况下7.84LH2S的物质的量为:$\frac{7.84L}{22.4L/mol}$=0.35mol,11.2LO2的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,
氧化产物为硫或二氧化硫或SO2、S,还原产物只有H2O,其中生成水的质量为:m(H2O)=0.35mol×18g/mol=6.3g,
混合气体的总质量减去生成的水的质量为容器中氧化产物的质量,故容器中氧化产物的总质量为:34g/mol×0.35mol+0.5mol×32g/mol-6.3g=21.6g,
故答案为:21.6.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
12.下列实验过程中,始终无明显现象的是( )
| A. | 在稀硫酸中加入铜粉,再加入KNO3固体 | |
| B. | SO2通入Ba(NO3)2溶液中 | |
| C. | CO2通入CaCl2溶液中 | |
| D. | 稀盐酸滴加到Fe(OH)3胶体溶液中 |
7.下列有关物质应用的说法正确的是( )
| A. | 小苏打是面包发酵粉的主要成分之一 | |
| B. | 盐类都可用作调味品 | |
| C. | 铝罐可久盛食醋 | |
| D. | 生石灰用作食品抗氧化剂 |
14.下面的原子或原子团不属于官能团的是( )
| A. | NO3- | B. | -Cl | C. | -OH | D. | 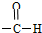 |
11.某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )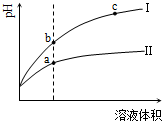

| A. | Ⅱ为盐酸稀释时的pH变化曲线 | |
| B. | a点Kw的数值比c点Kw的数值大 | |
| C. | b点酸的总浓度小于a点酸的总浓度 | |
| D. | b点溶液的导电性比c点溶液的导电性强 |
8.在1L 1mol/L的氨水中,下列说法正确的是( )
| A. | 含1 mol NH3分子 | B. | 含NH3和NH4+之和为1mol | ||
| C. | 含NH3、NH4+、NH3•H2O之和为1 mol | D. | 含NH3•H2O 1mol |
6.对烷烃CH3CH(C2H5)CH(C2H5)CH(CH3)2的命名,正确的是( )
| A. | 2,3-二甲基-4-乙基戊烷 | B. | 2-甲基3,4-二乙基戊烷 | ||
| C. | 2,4-二甲基-3-乙基己烷 | D. | 2,5-二甲基-3-乙基己烷 |