题目内容
下列说法正确的是( )
| A、AgCl难溶于水,是非电解质 |
| B、NaCl溶液在通电的条件下电离成Na+和Cl- |
| C、强电解质溶液导电能力一定强于弱电解质溶液导电能力 |
| D、强电解质在固态或液态时,可能不导电 |
考点:电解质与非电解质,强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.氯化银在溶于水或在熔融时能电离,故是电解质;
B.电离是在溶于水或熔融时发生的,不是通电后发生的;
C.溶液的导电能力与离子浓度成正比,与电解质的强弱无关;
D.强电解质在固态或液态时可能不导电,因为可能未电离.
B.电离是在溶于水或熔融时发生的,不是通电后发生的;
C.溶液的导电能力与离子浓度成正比,与电解质的强弱无关;
D.强电解质在固态或液态时可能不导电,因为可能未电离.
解答:
解:A.氯化银虽难溶,但溶于水的部分或在熔融时能完全电离,故是电解质,且为强电解质,故A错误;
B.电离是在溶于水或熔融时发生的,不是通电后发生的,故B错误;
C.溶液的导电能力与离子浓度成正比,与电解质的强弱无关,故C错误;
D.强电解质在固态或液态时可能不导电,因为可能未电离,例如氯化钠固体、液态氯化氢,故D正确;
故选A.
B.电离是在溶于水或熔融时发生的,不是通电后发生的,故B错误;
C.溶液的导电能力与离子浓度成正比,与电解质的强弱无关,故C错误;
D.强电解质在固态或液态时可能不导电,因为可能未电离,例如氯化钠固体、液态氯化氢,故D正确;
故选A.
点评:本题考查电解质与非电解质,注意电解质的强弱与导电能力的关系,解答该类概念性题目,应对概念十分清晰.抓住概念中的关键词,是解答的关键.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
能正确表示下列化学反应的离子方程式的是( )
| A、澄清的石灰水与硫酸的反应OH-+H+=H2O |
| B、氧化镁与硝酸(aq)反应O2-+2H+=H2O |
| C、硫酸镁(aq)与氢氧化钡(aq)混合Ba2++SO42-=BaSO4↓ |
| D、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
下列说法错误的是( )
| A、从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L |
| B、制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况) |
| C、0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数为2×6.02×1023 |
| D、10g 98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的 |
用水稀释0.1mol/L氨水时,溶液中随着水量的增加而增大的是( )
A、
| ||||
B、
| ||||
| C、c(NH3?H2O) | ||||
| D、n(OH-) |
下列离子方程式书写正确的是( )
| A、碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、工业制漂白粉的反应:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O |
| C、用铜作电极电解饱和食盐水:2Cl-+2H2O=2OH-+Cl2↑+H2↑ |
| D、铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O |
对于相同质量的SO2和SO3,下列说法中正确的是( )
| A、硫元素的质量比为1:1 |
| B、氧元素的质量比为6:5 |
| C、电子总数之比为1:1 |
| D、物质的量之比为4:5 |
下列方法对2SO2(g)+O2(g)?2SO3(g)的反应速率没有影响的是( )
| A、加入SO3 |
| B、容积不变,充入N2 |
| C、压强不变,充入N2 |
| D、降低温度 |
下列关于浓硫酸的叙述正确的是( )
| A、浓H2SO4有氧化性,稀H2SO4无氧化性 |
| B、常温下能用铝制容器盛放浓硫酸 |
| C、浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 |
| D、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
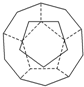 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.