题目内容
13.25℃时,下列溶液等体积混合后,溶液pH>7的是( )| A. | pH=3的H2SO4和pH=11的氨水 | |
| B. | 0.1 mol/L的盐酸和0.2 mol/L的醋酸钠溶液 | |
| C. | 等物质的量浓度的盐酸和氨水 | |
| D. | 等物质的量浓度的硫酸和NaOH溶液 |
分析 A.氨水为弱碱,混合液中氨水过量,溶液呈碱性;
B.反应后溶质为醋酸和氯化钠,溶液呈酸性;
C.二者恰好反应生成氯化铵,铵根离子水解溶液呈酸性;
D.硫酸为二元强酸,混合液中硫酸过量,溶液呈酸性.
解答 解:A.pH=3的H2SO4和pH=11的氨水等体积混合后,氨水过量,混合液呈碱性,溶液的pH>7,故A正确;
B.0.1 mol/L的盐酸和0.2 mol/L的醋酸钠溶液等体积混合,混合液醋酸和NaCl,溶液的pH<7,故B错误;
C.等物质的量浓度的盐酸和氨水等体积混合,反应后溶质为氯化铵,铵根离子水解溶液呈酸性,混合液的pH<7,故C错误;
D.等物质的量浓度的硫酸和NaOH溶液等体积混合,硫酸为二元酸,混合液中硫酸过量,溶液呈酸性,混合液的pH<7,故D错误;
故选A.
点评 本题考查溶液酸碱性与溶液pH的计算,题目难度不大,明确弱电解质的电离特点为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及综合应用能力.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
20.用透明胶带从石墨表面可以“剥离”出一种物质--石墨烯,它是世上最薄却也是最坚硬的材料,未来可用于生产超级计算机.关于石墨烯的说法正确的是( )
| A. | 石墨烯与金刚石互为同位素 | B. | 石墨烯属于烯烃 | ||
| C. | 石墨烯是单质 | D. | 石墨烯不导电 |
4.下列溶液一定呈碱性的是( )
| A. | c(H+)<c(OH-)的溶液 | B. | 含有OH-的溶液 | C. | NaHSO3 | D. | FeCl3 |
1.某有机物的结构简式如图,关于该有机物的性质叙述不正确的是( )


| A. | 能与溴的四氯化碳溶液发生加成反应 | |
| B. | 能与碳酸钠溶液反应 | |
| C. | 不能使酸性高锰酸钾溶液褪色 | |
| D. | 在一定条件下可以发生加聚反应生成高分子化合物 |
18.下列物质中,含有非极性共价键的是( )
| A. | Cl2 | B. | HCl | C. | NaOH | D. | CH3Cl |
5.下列说法正确的是( )
| A. | 用酸性高锰酸钾溶液除去乙烷中混有的乙烯,从而得到纯净的乙烷气体 | |
| B. | 向溴水中加入一定量的CCl4并振荡,静置后出现分层现象,上层为橙红色溶液 | |
| C. | 除去乙酸乙酯中的乙醇和乙酸可以用烧碱溶液 | |
| D. | 油脂属于酯类物质,地沟油可用于生产肥皂或生物柴油 |
2.下列有关二氧化硫说法中正确的是( )
| A. | 二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加 | |
| B. | 二氧化硫能使品红褪色,加热后颜色不能恢复 | |
| C. | 二氧化硫使酸性高锰酸钾褪色,体现了二氧化硫的漂白性 | |
| D. | 二氧化硫属于碱性氧化物,可以用NaOH溶液吸收 |
10.下列装置应用于实验室进行相关实验,能达到实验目的是( )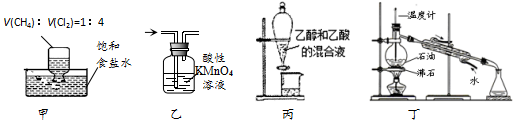

| A. | 用装置甲在光照条件下验证甲烷与氯气的反应 | |
| B. | 用装置乙除去甲烷中少量的乙烯得纯净甲烷 | |
| C. | 用装置丙分离乙醇和乙酸的混合液 | |
| D. | 用装置丁分馏石油并收集60~150℃馏分 |