题目内容
20.用1L0.5mol/L氢氧化钠溶液吸收0.4摩尔二氧化碳,所得溶液中的碳酸根离子和碳酸氢根离子的物质的量浓度之比约是( )| A. | 3:1 | B. | 1:2 | C. | 2:3 | D. | 1:3 |
分析 用1L0.5mol•L-1NaOH溶液吸收0.4molCO2,氢氧化钠的物质的量为0.5mol,氢氧化钠和二氧化碳的物质的量之比为5:4,则所得产物有Na2CO3和NaHCO3,然后根据Na元素和C元素守恒列式计算.
解答 解:用1L0.5mol•L-1NaOH溶液吸收0.4molCO2,氢氧化钠和二氧化碳的物质的量之比=(0.5mol/L×1L):0.4mol=5:4,则所得产物有Na2CO3和NaHCO3,
设CO32-和HCO3-的物质的量分别为x、y,
根据碳原子和钠离子守恒可得:x+y=0.4mol、2x+y=0.5mol,
解得:x=0.1mol、y=0.3mol,
同一溶液中浓度之比等于物质的量之比,
则所得溶液中的CO32-和HCO3-的物质的量浓度之比约是0.1mol:0.3mol=1:3,
故选D.
点评 本题考查了物质的量浓度的计算,题目难度中等,正确判断反应产物为解答关键,注意掌握守恒思想在化学计算能力中的应用方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
20.下列离子中不含配位键的是( )
| A. | Ag(NH3)2+ | B. | NH4+ | C. | OH- | D. | O22- |
11.把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示.下列说法正确的是( )

| A. | 装置一中铁片的生锈速度比装置二要慢 | |
| B. | 装置一中Ⅰ电极上有气泡冒出 | |
| C. | 一段时间后,两个装置中II和IV电极附近出现红色 | |
| D. | 装置二中加入少量KSCN溶液,溶液变为血红色 |
8.下列操作正确的是( )
| A. |  测溶液pH | B. |  稀释浓硫酸 | C. |  干燥Cl2 | D. |  制氢氧化亚铁 |
15.下列图示与对应的叙述相符的是( )
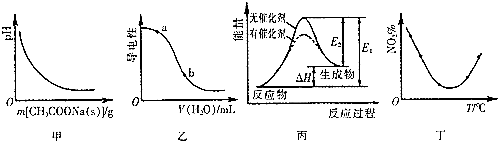

| A. | 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 图乙表示向NH3•H2O溶液中加水时溶液的导电性变化,则NH3•H2O溶液的pH:a<b | |
| C. | 图丙表示催化剂能改变化学反应的活化能 | |
| D. | 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则反应的△H>0 |
5.下列化合物分子中的所有原子一定处于同一平面的是( )
| A. | 乙烷 | B. | 苯乙烯 | C. | 氯乙烯 | D. | 丙烯 |
12.在N2O4(g)?2NO2(g)平衡体系中,增大N2O4的浓度,则NO2和N2O4的物质的量之比,下列叙述正确的是( )
| A. | 一定增大 | B. | 一定减小 | ||
| C. | 一定不变 | D. | 可能减小也可能不变 |
10.下列各组物质中,只要总质量一定,不论以何种比例混合,完全燃烧,生成的二氧化碳和水的质量也总是定值的是( )
| A. | 丙烷和丙烯 | B. | 乙烯和环丙烷 | C. | 乙炔和丁炔 | D. | 甲烷和乙烷 |



