题目内容
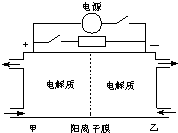 如图是一种蓄电池的示意图,被膜隔开的电解质分别为Na2S2和NaBr3.放电后变为Na2S4和NaBr下面对该装置工作过程中叙述正确的是( )
如图是一种蓄电池的示意图,被膜隔开的电解质分别为Na2S2和NaBr3.放电后变为Na2S4和NaBr下面对该装置工作过程中叙述正确的是( )| A、放电过程,甲电极电极反应:2S22--2e-=S42- |
| B、放电过程,电池反应:2S22-+Br3-=S42-+3Br- |
| C、充电过程,阳极室流出NaBr3溶液 |
| D、充电后向阳极室补充Na2S4溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、原电池正极发生还原反应,负极发生氧化反应,根据化合价的变化判断;
B、原电池中,正极和负极反应的和即为总反应;
C、电池充电时,阳极发生氧化反应,阴极发生还原反应;
D、充电时,阳离子向阴极移动,阴离子向阳极移动.
B、原电池中,正极和负极反应的和即为总反应;
C、电池充电时,阳极发生氧化反应,阴极发生还原反应;
D、充电时,阳离子向阴极移动,阴离子向阳极移动.
解答:
解:A、放电过程,甲电极是正极,发生得电子的还原反应,电极反应:Br3-+2e-=3Br-,故A错误;
B、总反应为Na2S2和NaBr3生成Na2S4和NaBr的反应,即2S22-+Br3-=S42-+3Br-,故B正确;
C、电池充电时,阳极发生氧化反应,电极反应为3NaBr-2e-=NaBr3+2Na+(或Br3-),即阳极室流出NaBr3溶液,故C正确;
D、电池充电时,阳极发生氧化反应,电极反应为3NaBr-2e-=NaBr3+2Na+(或Br3-),充电后向阳极室补充NaBr溶液,故D错误.
故选BC.
B、总反应为Na2S2和NaBr3生成Na2S4和NaBr的反应,即2S22-+Br3-=S42-+3Br-,故B正确;
C、电池充电时,阳极发生氧化反应,电极反应为3NaBr-2e-=NaBr3+2Na+(或Br3-),即阳极室流出NaBr3溶液,故C正确;
D、电池充电时,阳极发生氧化反应,电极反应为3NaBr-2e-=NaBr3+2Na+(或Br3-),充电后向阳极室补充NaBr溶液,故D错误.
故选BC.
点评:本题综合考查原电池和电解池知识,为高考常见题型,侧重于学生的分析能力的考查,难度较大,能正确写出电极反应式是该题的关键.

练习册系列答案
相关题目
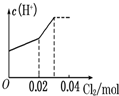
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO-与ClO
的浓度之比为1:3,则Cl2与NaOH溶液反应时参加反应的Cl2与被氧化的氯气的物质的量之比为( )
- 3 |
| A、21:5 | B、11:3 |
| C、3:1 | D、5:1 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、室温下,1L pH=1的盐酸中,由水电离的H+离子数目为0.1NA |
| B、标况下,11.2L SO3所含的分子数目为0.5NA |
| C、甲烷碱性燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA |
| D、1 mol C2H6O分子中含有的O-H键数目一定为NA |
下列有关反应限度的叙述正确的是( )
| A、平衡常数K的大小能说明反应的限度,因此当平衡右移时,K值必定增大 |
| B、可逆反应达到平衡状态后,改变外界条件后,若反应速率发生变化,则平衡一定发生移动 |
| C、若反应2A(g)+B(g)?2C(g)是自发反应,则该反应的△H<0 |
| D、使用催化剂可降低反应活化能,加快反应速率,改变反应限度 |
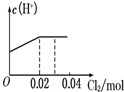
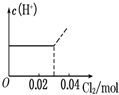
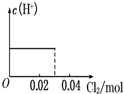
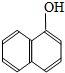
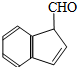
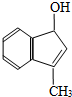
 .下列化合物中,不能与2一奈酚互为同分异构体的是( )
.下列化合物中,不能与2一奈酚互为同分异构体的是( )
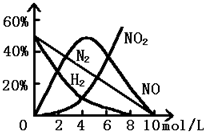 镁与硝酸的反应中,测得其气体产物有H2,NO,NO2,溶液中产物有Mg(NO3)2,NH4NO3和H2O,生成这些产物的HNO3的浓度范围为:
镁与硝酸的反应中,测得其气体产物有H2,NO,NO2,溶液中产物有Mg(NO3)2,NH4NO3和H2O,生成这些产物的HNO3的浓度范围为: