题目内容
9.下列说法正确的是( )| A. | 凡是放热反应都是自发的,吸热反应都是非自发的 | |
| B. | 常温下,C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 | |
| C. | 任何能使熵值增大的过程都能自发进行 | |
| D. | 反应物和生成物所具有的总焓决定了反应是否能自发进行 |
分析 放热反应有利于反应的自发进行,熵增加的饭应有利于反应的自发进行,但是化学反应能否自发进行的判据是看△H-T△S是否小于零.
解答 解:A.放热反应有利于反应的自发进行,但是不一定所有的放热反应都是自发反应,故A错误;
B.CO2(g)+C(s)?2CO(g)固体分解得到气体,混乱度增加,△S>0,不能自发进行,则△H-T•△S>0反应能进行,所以△H>0,故B正确;
C.化学反应能否自发进行的判据是:△H-T△S<0,必须综合考虑体系的焓变和熵变,不能单独根据熵变判断,故C错误;
D.反应物和生成物所具有的总焓相对大小决定了反应是放热还是吸热,但是不能判断反应能否自发进行,必须综合考虑体系的焓变和熵变来判断反应的自发性,故D错误.
故选B.
点评 本题考查学生影响化学反应方向的因素是:焓变和熵变,注意化学反应能否自发进行的判据是看△H-T△S是否小于零,必须综合考虑体系的焓变和熵变,题目难度不大.

练习册系列答案
相关题目
17.溶液、胶体和浊液这三种分散系的本质区别是( )
| A. | 是否为大量分子和离子的集合体 | B. | 能否通过滤纸或半透膜 | ||
| C. | 分散质粒子的大小 | D. | 是否均一、稳定、透明 |
4.下列物质分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaHSO4 ⑤液态氧 ⑥NaOH.
①纯碱 ②食盐水 ③石灰水 ④NaHSO4 ⑤液态氧 ⑥NaOH.
| A. | 盐--①④ | B. | 碱--①⑥ | C. | 纯净物--③④⑤ | D. | 混合物--②⑤ |
1.下列叙述正确的是(NA为阿伏加德罗常数的值)( )
| A. | 7.8gNa2O2含有的共价键数为0.2NA | |
| B. | 7.8gNa2S与Na2O2的混合物,含离子总数为0.3NA | |
| C. | 标准状况下,22.4L溴单质含有NA个溴分子 | |
| D. | 0.2 molNa被完全氧化生成7.8gNa2O2,转移电子的数目为0.4NA |
18.已知反应①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ/mol ②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol下列结论正确的是( )
| A. | 碳的燃烧热大于110.5 kJ/mol | |
| B. | ①反应的焓变为-221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
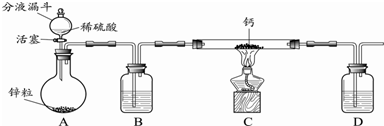
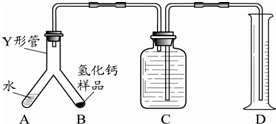

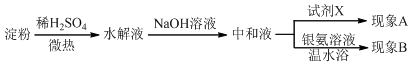
 可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: