题目内容
下列说法正确的是( )
| A、一定条件下可以用H2除去乙烷中混有的乙烯 |
| B、苯和四氯化碳都能萃取溴水中的溴 |
| C、乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法分离 |
| D、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
考点:物质的分离、提纯的基本方法选择与应用,有机物的结构和性质
专题:
分析:A.乙烯的含量不确定,易引入新杂质;
B.溴易溶于苯和四氯化碳;
C.乙醇、乙酸和乙酸乙酯混溶;
D.乙烯应用裂解的方法制备.
B.溴易溶于苯和四氯化碳;
C.乙醇、乙酸和乙酸乙酯混溶;
D.乙烯应用裂解的方法制备.
解答:
解:A.乙烯的含量不确定,易引入新杂质,可用溴水除杂,故A错误;
B.苯和四氯化碳不溶于水,且溴易溶于苯和四氯化碳,可用于萃取,故B正确;
C.乙醇、乙酸和乙酸乙酯混溶,应用蒸馏的方法分离,故C错误;
D.乙烯应用裂解的方法制备,故D错误.
故选B.
B.苯和四氯化碳不溶于水,且溴易溶于苯和四氯化碳,可用于萃取,故B正确;
C.乙醇、乙酸和乙酸乙酯混溶,应用蒸馏的方法分离,故C错误;
D.乙烯应用裂解的方法制备,故D错误.
故选B.
点评:本题考查物质的分离、提纯,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握有机物性质的异同,特别注意除杂时不能引入新杂质,难度不大.

练习册系列答案
相关题目
电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于元素电负性的变化规律正确的是( )
| A、周期表中从左到右,主族元素的电负性逐渐变大 |
| B、周期表中从上到下,同一主族元素的电负性逐渐变大 |
| C、电负性越大,金属性越强 |
| D、电负性越小,非金属性越强 |
a mL三种气态烃的混合物和足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),气体体积共缩小2a mL(不考虑二氧化碳的溶解).则三种烃可能的组合是( )
| A、相同条件下CH4、C2H4、C3H4任意体积比 |
| B、CH4、C3H6、C2H2保持C3H6:C2H2=1:2(物质的量之比) |
| C、C2H6、C4H6、C2H2同条件下体积比为2:1:1 |
| D、C3H8、C4H8、C2H2质量比为11:14:26 |
下列物质与其用途完全符合的有( )
①Al(OH)3-抗酸药 ②Si-太阳能电池 ③AgI-人工降雨
④NaCl-制纯碱 ⑤NaClO-消毒剂 ⑥Al 和Fe2O3-焊接钢轨
⑦Fe2O3-红色油漆或涂料 ⑧MgO-耐火材料.
①Al(OH)3-抗酸药 ②Si-太阳能电池 ③AgI-人工降雨
④NaCl-制纯碱 ⑤NaClO-消毒剂 ⑥Al 和Fe2O3-焊接钢轨
⑦Fe2O3-红色油漆或涂料 ⑧MgO-耐火材料.
| A、5条 | B、6条 | C、7条 | D、8条 |
在相同条件下,下列气态氢化物的稳定性排列顺序正确的是( )
| A、HF>HCl>HBr>HI |
| B、HCl>HBr>HI>HF |
| C、HBr>HI>HF>HCl |
| D、HI>HBr>HCl>HF |
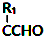 +H2O(R、R1表示炔基或氢)
+H2O(R、R1表示炔基或氢)