题目内容
氢气作为一种具有广阔开发前景的新型能源,具有生产周期短,燃烧产物无污染等优点.城市管道煤气的主要成分是CO,充分燃烧后的产物CO2也不会造成空气污染.某工厂在炼焦过程中的副产品水煤气(C+H2O CO+H2),也可作为气体燃料.
CO+H2),也可作为气体燃料.
(1)现有V m3标准状况下的CO和H2的混合气体,充分燃烧时,需标准状况下氧气的体积为________m3,若将空气的成分视为V(N2)∶V(O2)=4∶1,则所需标准状况下空气的体积为________m3.
(2)某温度下,m g下列物质:①H2;②CO;③CO和H2的混合气体;④醋酸(CH3COOH);⑤甲醛(HCHO);⑥甲酸甲酯(HCOOCH3).分别与足量的O2充分反应,并将燃烧产物(CO2和H2O)立即与过量的Na2O2反应.反应后测得Na2O2固体增重m g,则符合上述要求的物质是
[ ]
A.①②③
B.④⑤⑥
C.①③⑤⑥
D.①②③④⑤⑥
答案:0.5V,2.5V;D
解析:
解析:
|
(1)0.5V,2.5V;(2)D 导解:根据相关的化学方程式,并利用差量法,可以推知,不论是H2还是CO,或者是H2和CO的混合气体,甚至不是H2或CO,但只要其组成可以改写成(CO)m(H2)n的形式的,均符合题目中相关质量的变化情况. |

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
(15分)科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是 。(选填字母)
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |

(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式: 。
(4)利用氢气和CO合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)
 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1② 2CH3OH(g)
 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1③ CO(g) + H2O(g)
 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1总反应:3H2(g) + 3CO(g)
 CH3OCH3(g) + CO2 (g)的ΔH=
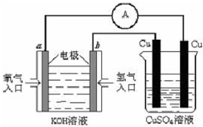
CH3OCH3(g) + CO2 (g)的ΔH= (5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①氢氧燃料电池中,正极的电极反应式为 。
②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为
L。
(6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式 。

 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1