题目内容
【选修3:物质结构与性质】(15分)
(1)亚铜离子(Cu+)基态时的价电子排布式表示为 。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为 (用元素符号表示)。
(3)Cu晶体的堆积方式是 (填堆积方式名称),其配位数为 ;往Cu的硫酸盐溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,下列说法正确的是_____
A.[Cu (NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Cu(NH3)4 ]2+中Cu2+给出孤对电子,NH3提供空轨道
C.[Cu (NH3)4]SO4组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为正四面体
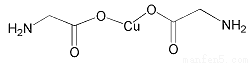
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为 。
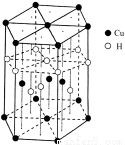
(5)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如下图所示。则该化合物的化学式为 。
(1)3d10(2分)(2)Br〉As〉Se(2分)
(3)面心立方最密堆积(2分); 12 (2分); A、D(2分);
(4)sp3 杂化 sp2杂化(2分) (5)CuH(3分)
【解析】
试题分析:(1)亚铜离子(Cu+)基态时的价电子排布式表示为3d10;(2)硒为第4周期元素,相邻的元素有砷和溴,一般情况下同一周期的元素,元素的原子序数越大,越大的电离能就越大,但是由于As原子的最外层电子处于该轨道的半充满的稳定状态,所以失去电子比原子序数比它大1的同一周期的氧族元素的还大,因此则3种元素的第一电离能从大到小顺序为Br〉As〉Se;(3)Cu晶体的堆积方式是面心立方最密堆积;其配位数为12;往Cu的硫酸盐溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,A.该化合物是离子化合物,在[Cu (NH3)4]SO4中含有的化学键有离子键、极性键和配位键,正确;B.在[Cu(NH3)4 ]2+中NH3给出孤对电子,Cu2+提供空轨道,错误;C.[Cu (NH3)4]SO4组成元素中第一电离能最大的是氮元素,错误;D.SO42-与PO43-互为等电子体,空间构型均为正四面体,正确。(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为饱和碳原子是sp3 杂化,不饱和碳原子是sp2杂化;(5)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如右图所示。在每个晶胞中含有Cu: 12×1/6+2×1/2+3=6;H:6×1/3+1+3=6,n(Cu):n(H)=1:1,所以该化合物的化学式为CuH。
考点:考查离子核外电子排布式、金属Cu的堆积方式、配位数、物质内的化学键、原子的杂化、等电子体、、元素的电离能的比较、晶体化学式的确定的知识。

下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe 2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
 、K+
、K+ +H2O
+H2O CO2(g) + 3H2(g)
CO2(g) + 3H2(g) 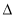 H(298K)=+ 49.4 kJ/mol
H(298K)=+ 49.4 kJ/mol H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b _______ 1(填“﹤”、“﹥”或“=”) 。
H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b _______ 1(填“﹤”、“﹥”或“=”) 。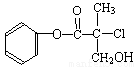 。下列叙述正确的是
。下列叙述正确的是 ”的且只含一个官能团的同分异构体有( )。
”的且只含一个官能团的同分异构体有( )。