题目内容
5.含有CO、N2、H2、CO2和少量水蒸气的混合气体,依次通过足量的灼热氧化铜、浓氢氧化钠溶液、浓硫酸后,剩余的气体是( )| A. | N2 | B. | N2和H2 | C. | N2和CO2 | D. | H2和CO |
分析 CO、N2、H2、CO2中,CO、H2可与CuO在加热条件下反应,CO2可与氢氧化钠溶液反应,水可被浓硫酸吸收,以此解答该题.
解答 解:含有CO、N2、H2、CO2和少量水蒸气的混合气体,依次通过足量的灼热氧化铜,CO、H2反应分别生成二氧化碳和水,二氧化碳可与浓氢氧化钠溶液反应,浓硫酸可吸收水,则剩余气体为氮气.
故选A.
点评 本题综合考查常见气体的性质,为高频考点,侧重考查学生的分析能力和实验能力,注意把握物质的性质,难度不大.

练习册系列答案
相关题目
15.下列微粒中同时具有离子键、共价键和配位键的化合物是( )
| A. | NH4Cl | B. | Na2O2 | C. | H3O+ | D. | MgO |
16.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是氯碱工业的主要原料.下列说法正确的是( )
| A. | C和E的单质常温下不能相互反应 | |
| B. | C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同 | |
| C. | 原子半径:C>D>A>B | |
| D. | A、D、E的最高价氧化物对应水化物均为弱酸 |
13. X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )
X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )
 X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )
X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )| A. | 该过程所涉及的反应均为氧化还原反应 | |
| B. | 当X单质为金属时,可能是Na或Fe | |
| C. | 当X单质为非金属时,可能是F2或 C | |
| D. | 反应①可能在常温下进行,也可能需要在高温下才能发生 |
20.下列装置或操作能达到实验目的是( )
| A. | .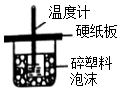 装置用于中和热的测定 | |
| B. | 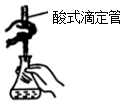 装置用于高锰酸钾溶液滴定草酸 | |
| C. | 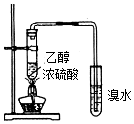 装置用于制取乙烯并验证乙烯的性质 | |
| D. | 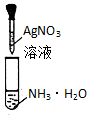 装置用于配制银氨溶液 |
10.能在水溶液中大量共存的一组离子是( )
| A. | H+、Fe3+、I-、SO${\;}_{4}^{2-}$ | B. | OH-、Na+、HCO${\;}_{3}^{-}$、Cl- | ||
| C. | K+、Ca2+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$ | D. | K+、Na+、OH-、AlO${\;}_{2}^{-}$ |
17.在强酸性溶液中,下列离子组能大量共存且溶液无色透明的是( )
| A. | Ag+、Na+、Cl-、K+ | B. | Na+、Fe2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
14.能与SO2气体发生反应,但无沉淀产生的是( )
①氯水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液 ⑤稀硫酸 ⑥Na2SO3溶液.
①氯水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液 ⑤稀硫酸 ⑥Na2SO3溶液.
| A. | 只有① | B. | ①③④ | C. | ④⑤⑥ | D. | ①④⑥ |
1.以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
| A. | 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3:2:1 | |
| B. | n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为$\frac{35.5m}{n}$ | |
| C. | 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 | |
| D. | 5.6 g CO和22.4 L CO2中含有的碳原子数一定相等 |