题目内容
完全燃烧等物质的量的某种有机物A和乙醇,所用的氧气的量相等。此时乙醇反应生成的水是A反应生成水的1.5倍。但A生成的二氧化碳的量又是乙醇生成二氧化碳的量的1.5倍,则此有机物A是( )A.CH3CH2CHO B.CH3OCH2CH
解析:由乙醇的燃烧方程式:CH3CH2OH+3O2![]() 2CO2+3H2O推知,1 mol A可生成水2 mol,生成CO2为3 mol,即含有氢原子4 mol,其分子式为C3H4O2。
2CO2+3H2O推知,1 mol A可生成水2 mol,生成CO2为3 mol,即含有氢原子4 mol,其分子式为C3H4O2。
答案:C

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
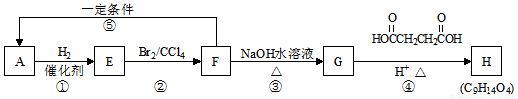
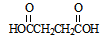 )与乙二醇(HOCH2CH2OH)在催化剂作用下,经聚合反应可制成一种新型可生物降解的高分子材料。请写出该聚合物的结构简式:
)与乙二醇(HOCH2CH2OH)在催化剂作用下,经聚合反应可制成一种新型可生物降解的高分子材料。请写出该聚合物的结构简式: