题目内容
 科学研究发现Cu2O可作为太阳光分解水的催化剂.
科学研究发现Cu2O可作为太阳光分解水的催化剂.Ⅰ.通过以下四种方法来制备Cu2O.
a.火法还原:用炭粉在高温条件下还原CuO;
b.用CH3CHO还原新制的Cu(OH)2:
c.电解法:2Cu+H2O
| ||
d.最新实验研究用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2;该法的化学方程式为
Ⅱ.用制得的Cu2O进行催化分解水的实验.
(1)一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:2H2O(g)═2H2g)+O2(g)△H=+484kJ/mol.测得不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
(2)用以上四种方法制得的Cu2O在相同条件下分别对水进行催化分解,产生氢气的体积V(H2)随时间t变化如图所示,则下列说法正确的是
A.c、d方法制得的Cu2O催化效率相对较高
B.d方法制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有关
D.分解等物质的量的水时,d方法制得的Cu2O作催化剂所需吸收的能量最低.
考点:浓度、温度、催化剂对化学反应速率的影响
专题:化学反应速率专题
分析:Ⅰ.根据反应物和生成物结合质量守恒书写化学方程式;
Ⅱ.(1)根据化学反应速率之比等于计算数之比计算反应速率,达平衡时,生成氧气0.002mol,根据热化学方程式计算;
(2)根据图象曲线的变化趋势判断,曲线斜率越大,反应速率越大,温度升高,斜率逐渐减小,以此解答.
Ⅱ.(1)根据化学反应速率之比等于计算数之比计算反应速率,达平衡时,生成氧气0.002mol,根据热化学方程式计算;
(2)根据图象曲线的变化趋势判断,曲线斜率越大,反应速率越大,温度升高,斜率逐渐减小,以此解答.
解答:
解:Ⅰ.用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2,反应的方程式为4Cu(OH)2+N2H4
2Cu2O+N2+6H2O,
故答案为:4Cu(OH)2+N2H4
2Cu2O+N2+6H2O;
Ⅱ.(1)由表中数据可知前20min时v(O2)=
=2.5×10-5 mol.L-1.min -1,则v(H2O)=2v(O2)=5.0×10-5 mol.L-1.min -1,
达平衡时,生成氧气0.002mol,至少需要吸收的光能为0.002mol×484kJ?mol-1=0.968kJ,
故答案为:5.0×10-5 mol?L-1?min-1;0.968;
(2)A.c、d曲线斜率较大,说明反应速率较大,则c、d方法制得的Cu2O催化效率相对较高,故A正确;
B.催化剂只改变反应速率,不影响平衡移动,故B错误;
C.用不同的方法制备的氧化亚铜的颗粒大小不同,由图象可知催化效果不同,则催化效果与Cu2O颗粒的粗细、表面活性等有关,故C正确;
D.温度升高,斜率逐渐减小,说明Cu2O催化水分解时,需要适宜的温度,分解等物质的量的水时,d方法制得的氢气最多,因此Cu2O作催化剂所需吸收的能量最高,故D错误;
故答案为:AC.
| ||
故答案为:4Cu(OH)2+N2H4
| ||
Ⅱ.(1)由表中数据可知前20min时v(O2)=
| 0.0010mol | ||
|
达平衡时,生成氧气0.002mol,至少需要吸收的光能为0.002mol×484kJ?mol-1=0.968kJ,
故答案为:5.0×10-5 mol?L-1?min-1;0.968;
(2)A.c、d曲线斜率较大,说明反应速率较大,则c、d方法制得的Cu2O催化效率相对较高,故A正确;
B.催化剂只改变反应速率,不影响平衡移动,故B错误;
C.用不同的方法制备的氧化亚铜的颗粒大小不同,由图象可知催化效果不同,则催化效果与Cu2O颗粒的粗细、表面活性等有关,故C正确;
D.温度升高,斜率逐渐减小,说明Cu2O催化水分解时,需要适宜的温度,分解等物质的量的水时,d方法制得的氢气最多,因此Cu2O作催化剂所需吸收的能量最高,故D错误;
故答案为:AC.
点评:本题考查较为综合,涉及氧化亚铜的制备方案、电解、化学平衡以及反应速率的影响等知识,侧重于学生的分析能力的考查,为高考常见题型,题目难度中等.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
化学与人类生产、生活、社会可持续发展密切相关.下列有关说法正确的是( )
| A、高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2═2O3有单质参加,属于氧化还原反应 |
| B、人造纤维,合成纤维和光导纤维都是有机高分子化合物 |
| C、大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨 |
| D、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
从葡萄籽中提取的原花青素结构为:有关原花青素的下列说法不正确的是( )
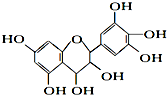

| A、该物质既可看作醇类,也可看作酚类 |
| B、1mol该物质可与4mol Br2反应 |
| C、1mol该物质可与7mol Na反应 |
| D、1mol该物质可与7mol NaOH反应 |
生活中处处有化学.下列说法正确的是( )
| A、煎炸食物的花生油和牛油都是可皂化的饱和酯类 |
| B、做衣服的棉和麻均与淀粉互为同分异构体 |
| C、制饭勺、饭盒、高压锅等的不锈钢是合金 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
关于下列实验装置的叙述中,正确的是( )
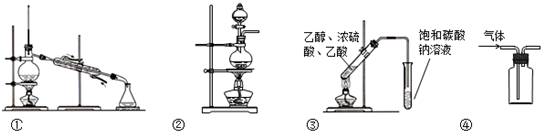

| A、装置①常用于分离互不相溶的液体 |
| B、装置②可用于实验室加热酒精与浓硫酸的混合物制取乙烯 |
| C、装置③可用于制备乙酸乙酯 |
| D、装置④可用于收集NO、CO2等气体 |
 前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.
前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.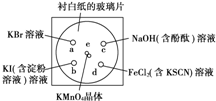 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol?L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,各种液滴彼此分开,围成半径小于表面皿的圆形(如图所示)在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol?L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,各种液滴彼此分开,围成半径小于表面皿的圆形(如图所示)在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.