题目内容
下列事实不能用勒夏特列原理解释的是( )
| A、用浓氨水和氢氧化钠制取氨气 |
| B、加热蒸干AlCl3溶液不能得到无水AlCl3 |
| C、工业上SO2和O2在常压下生成SO3 |
| D、水中的c(H+)比0.1 mol/LNaOH溶液中的大 |
考点:化学平衡移动原理
专题:
分析:勒夏特利原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,勒夏特利原理适用的对象应存在可逆过程,如与可逆过程的平衡移动无关,则不能用勒夏特利原理解释.
解答:
解:A.NH3+H2O?NH3?H2O?NH4++OH-,加入氢氧化钠,增大氢氧根离子浓度,平衡逆向移动,有利于氨气的生成,故能用勒夏特列原理解释,故A不选;
B.AlCl3水解存在平衡AlCl3+3H2O?Al(OH)3(胶体)+3HCl,加热HCl挥发,水解彻底进行,生成Al(OH)3沉淀,灼烧Al(OH)3得Al2O3,能用勒夏特列原理解释,故B不选;
C.2SO2+O2?2SO3,增大压强,平衡正向移动,常压下不利于生成SO3,故不能用勒夏特列原理解释,故C选;
D.水中存在电离平衡:H2O?H++OH-,加入氢氧化钠,增大氢氧根离子浓度,平衡逆向移动,氢离子浓度减小,故能利用平衡移动原理解释,故D不选,
故选C.
B.AlCl3水解存在平衡AlCl3+3H2O?Al(OH)3(胶体)+3HCl,加热HCl挥发,水解彻底进行,生成Al(OH)3沉淀,灼烧Al(OH)3得Al2O3,能用勒夏特列原理解释,故B不选;
C.2SO2+O2?2SO3,增大压强,平衡正向移动,常压下不利于生成SO3,故不能用勒夏特列原理解释,故C选;
D.水中存在电离平衡:H2O?H++OH-,加入氢氧化钠,增大氢氧根离子浓度,平衡逆向移动,氢离子浓度减小,故能利用平衡移动原理解释,故D不选,
故选C.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.

练习册系列答案
相关题目
下列关于Na2O和Na2O2的叙述正确的是( )
| A、都是白色的固体 |
| B、都是碱性氧化物 |
| C、都是强氧化剂 |
| D、都能与水反应形成强碱溶液 |
下列说法正确的是( )
| A、可用加热的方法除去混在碳酸钠固体中的碳酸氢钠固体 |
| B、除去镁粉中少量的铝粉,可选用NaOH溶液 |
| C、向某溶液中加入盐酸,产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32- |
| D、向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中一定含有SO42- |
下列有关金属及其化合物的说法正确的是( )
| A、Na久置于空气中最终生成NaHCO3 |
| B、Mg比Al活泼,更易与NaOH溶液反应生成H2 |
| C、水蒸气通过灼热的铁粉有红棕色固体生成 |
| D、铜粉与稀硫酸不反应,加入一定量硝酸钠后铜粉溶解 |
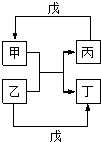 甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )
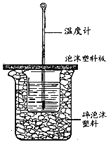 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题: