题目内容
ZnSe是一种光电性能优异的半导体材料,人们开发出了多种制备ZnSe纳米粒子的方法.某研究小组用如下方法制备了ZnSe纳米粒子:

(1)SeO2能溶于水,溶解过程中的化学方程式:
(2)硒酸(H2SeO4)的水溶液按下式发生一级和二级电离:
H2SeO4=H++HSeO4-;HSeO4- H++SeO42-,K2=1.0×10-2(298K)
H++SeO42-,K2=1.0×10-2(298K)
Na2SeO4溶液显
(3)已知肼(N2H4)有强还原性,在反应釜中与SeO32-反应的氧化产物是N2,请写出该反应的离子程式:
(4)使用合适的催化剂和电极材料,以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,同时达到固氮作用.该电池的正极反应式为

(1)SeO2能溶于水,溶解过程中的化学方程式:
SeO2+H2O═H2SeO3
SeO2+H2O═H2SeO3
;(2)硒酸(H2SeO4)的水溶液按下式发生一级和二级电离:
H2SeO4=H++HSeO4-;HSeO4-
 H++SeO42-,K2=1.0×10-2(298K)
H++SeO42-,K2=1.0×10-2(298K)Na2SeO4溶液显
碱性
碱性
(填“酸性”、“中性”、“碱性”).理由SeO42-+H2O═HSeO4-+OH-
SeO42-+H2O═HSeO4-+OH-
(用离子方程式表示)(3)已知肼(N2H4)有强还原性,在反应釜中与SeO32-反应的氧化产物是N2,请写出该反应的离子程式:
2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O
2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O
.(4)使用合适的催化剂和电极材料,以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,同时达到固氮作用.该电池的正极反应式为
N2+6e-+8H+=2NH4+
N2+6e-+8H+=2NH4+
.分析:(1)Se与S同主族,SeO2为酸性氧化物,与SO2性质相似;
(2)根据HSeO4- H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性;
H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性;
(3)在反应釜中反应物有Zn2+、SeO32-、N2H4,生成物有N2,根据氧化还原反应得失电子相等和质量守恒定律书写离子方程式;
(4)原电池正极发生还原反应.
(2)根据HSeO4-
 H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性;
H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性;(3)在反应釜中反应物有Zn2+、SeO32-、N2H4,生成物有N2,根据氧化还原反应得失电子相等和质量守恒定律书写离子方程式;
(4)原电池正极发生还原反应.
解答:解:(1)SeO2为酸性氧化物,与水反应生成H2SeO3,反应方程式为SeO2+H2O═H2SeO3,故答案为:SeO2+H2O═H2SeO3;
(2)根据HSeO4- H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性,水解离子方程式为SeO42-+H2O═HSeO4-+OH-,
H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性,水解离子方程式为SeO42-+H2O═HSeO4-+OH-,
故答案为:碱性;SeO42-+H2O═HSeO4-+OH-;
(3)在反应釜中反应物有Zn2+、SeO32-、N2H4,生成物有N2,SeO32-被还以为-2价的Se,与Zn2+生成ZnSe,根据氧化还原反应得失电子相等和质量守恒定律,离子方程式为
2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O,故答案为:2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O;
(4)以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,正极发生还原反应,即氮气被还原生成NH4+,电极反应式为N2+6e-+8H+=2NH4+,故答案为:N2+6e-+8H+=2NH4+.
(2)根据HSeO4-
 H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性,水解离子方程式为SeO42-+H2O═HSeO4-+OH-,
H++SeO42-,K2=1.0×10-2(298K),可知Na2SeO4为强碱弱酸盐,SeO42-离子水解,溶液呈碱性,水解离子方程式为SeO42-+H2O═HSeO4-+OH-,故答案为:碱性;SeO42-+H2O═HSeO4-+OH-;
(3)在反应釜中反应物有Zn2+、SeO32-、N2H4,生成物有N2,SeO32-被还以为-2价的Se,与Zn2+生成ZnSe,根据氧化还原反应得失电子相等和质量守恒定律,离子方程式为
2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O,故答案为:2Zn2++2SeO32-+3N2H4=2ZnSe+3N2↑+6H2O;
(4)以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,正极发生还原反应,即氮气被还原生成NH4+,电极反应式为N2+6e-+8H+=2NH4+,故答案为:N2+6e-+8H+=2NH4+.
点评:本题考查较为综合,涉及氧化还原反应、原电池等知识,本题难度中等,本题易错点为(3),注意判断反应物和生成物,用守恒的方法书写离子方程式.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案
相关题目
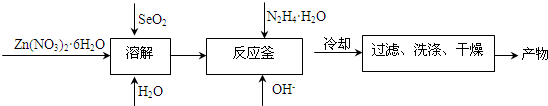
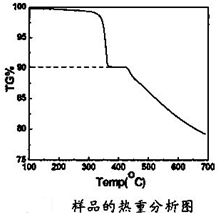 (4)将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1,N和H的原子个数比为1:2; 产物样品经红外光谱分析可知产物中含有N-H、N-N键.结合产物样品的热重(重量-温度关系图)分析结果如图所示,推测产物的化学式可能为:
(4)将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1,N和H的原子个数比为1:2; 产物样品经红外光谱分析可知产物中含有N-H、N-N键.结合产物样品的热重(重量-温度关系图)分析结果如图所示,推测产物的化学式可能为: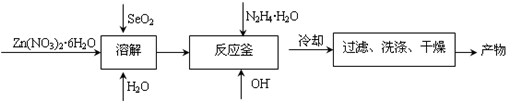


 H++SeO42-,K2=1.0×10-2(298K)
H++SeO42-,K2=1.0×10-2(298K)