题目内容
奥运会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生化学反应:5KClO3+6P=3P2O5十5KCl.而我国古代“火药”的成分是木炭粉(C)、硫磺(S)、硝石(KNO3),经点燃发生的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,则下列有关叙述中错误的是( )
| A、两个反应中还原产物前者为KCl,后者为K2S和N2 |
| B、两个反应均为置换反应 |
| C、若两个反应中生成等物质的量的P2O5和CO2转移电子数之比为5:2 |
| D、火药中的钾盐均作氧化剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:5KClO3+6P=3P2O5十5KCl中,Cl元素的化合价降低,P元素的化合价升高;
S+2KNO3+3C=K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素的化合价升高,以此来解答.
S+2KNO3+3C=K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素的化合价升高,以此来解答.
解答:
解:A.氧化剂对应还原产物,两个反应中Cl、S、N元素的化合价降低,则得到电子被还原,所以两个反应中还原产物前者为KCl,后者为K2S和N2,故A正确;
B.两个反应均不符合单质与化合物反应生成新单质与新化合物,均不属于置换反应,故B错误;
C.生成等物质的量的P2O5和CO2,设均为3mol,结合反应可知转移电子数之比为3mol×2×(5-0):3mol×(4-0)=5:2,故C正确;
D.氯酸钾中Cl元素、硝酸钾中N元素的化合价均降低,则火药中的钾盐均作氧化剂,故D正确;
故选B.
B.两个反应均不符合单质与化合物反应生成新单质与新化合物,均不属于置换反应,故B错误;
C.生成等物质的量的P2O5和CO2,设均为3mol,结合反应可知转移电子数之比为3mol×2×(5-0):3mol×(4-0)=5:2,故C正确;
D.氯酸钾中Cl元素、硝酸钾中N元素的化合价均降低,则火药中的钾盐均作氧化剂,故D正确;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从化合价角度分析解答,题目难度不大.

练习册系列答案
相关题目
下列各组微粒按半径逐渐增大,还原性逐渐增强的顺序排列的是( )
| A、Na、K、Rb |
| B、F、Cl、Br |
| C、Mg2+、Al3+、Zn2+ |
| D、Cl-、Br-、I- |
下列物质的立体结构与NH3相同的是( )
| A、H2O |
| B、CH4 |
| C、CO2 |
| D、H3O+ |
下列叙述正确的是( )
| A、通常把铝粉和氧化铁的混合物叫铝热剂 |
| B、某物质中只含有一种元素,该物质一定是纯净物 |
| C、40K和40Ca的中子数相等、质子数不相等 |
| D、乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键键能的两倍 |
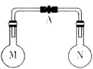 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A、①②③④ | B、①④③② |
| C、②④①③ | D、④①②③ |
下列分子或离子中键角由大到小排列顺序是( )
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2.
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2.
| A、⑤④①③ | B、⑤①④②③ |
| C、④①②⑤③ | D、③②④①⑤ |