题目内容
某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6mol的SO32-离子完全氧化,则X2O72-离子还原后X的化合价为
A.+1 B.+2 C.+4 D.+3
D
【解析】
试题分析:在氧化还原反应中元素化合价升降总数相等。假设X2O72-离子还原后X的化合价为+x价,则2(6-x)×0.2=0.6(6-4).解得x=+3价,因此选项是D。
考点:考查守恒方法在确定物质的化学式及氧化还原反应的计算中的应用的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案无机化合物可根据其组成和性质进行分类:
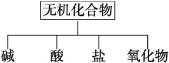
(1)上图所示的物质分类方法名称是 。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
物质 类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 | ①HCl ②____ | ③______ ④Ba(OH)2 | ⑤Na2CO3 ⑥_____ | ⑦CO2 ⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式
。
(4)实验室制备⑦常用 和 反应,检验该气体的方法是 。
图中各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲是发酵粉的主要成分,乙是一种常用的化肥,B、D常温常压下是气体。请回答下列问题: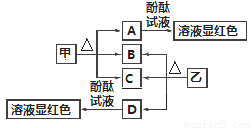
(1)甲的俗名是________。
(2)A、D物质的水溶液分别滴入酚酞试液后,溶液均显红色,其原理________(填“相同”或“不相同”)。
(3)甲在潮湿的空气中会缓慢分解,A会吸收空气中的水分:A+nH2O===A·nH2O(n为平均值,n≤10),取没有妥善保管的甲样品9.16 g,溶于水制成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的B的体积(标准状况)如下表:(溶于水中的B不计)
盐酸的体积(mL) | 4 | 8 | 15 | 20 | 50 | 120 | 150 |
生成B的体积(mL) | 0 | 0 | 112 | 224 | 896 | 2240 | 2240 |
则:
① 稀盐酸的物质的量浓度为__________________________________。
② 样品中的成分及其物质的量分别为__________________________________。
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
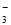 、K+
、K+ +H2O
+H2O