题目内容
17.质量数为A,核内中子数为N的R2+离子与16O所形成的Wg氧化物中所含质子的物质的量为( )| A. | $\frac{W}{A+16}$(A-N+8)mol | B. | $\frac{W}{A+16}$(A-N+10)mol | C. | (A-N+8)mol | D. | $\frac{W}{A}$(A-N+6)mol |
分析 核内中子数为N的R2+离子,质量数为A,所以质子数为A-N,该离子带2个单位正电荷,所以其氧化物的化学式为RO,根据n=$\frac{m}{M}$计算Wg该氧化物的物质的量,一个氧化物分子中含有(A-N+8)个质子,进而计算质子物质的量.
解答 解:该离子带2个单位正电荷,所以其氧化物的化学式为RO,该氧化物的摩尔质量为(A+16)g/mol,w g 它的氧化物的物质的量为$\frac{Wg}{(A+16)g/mol}$,
核内中子数为N的R2+离子,质量数为A,所以质子数为A-N,一个氧化物分子中含有(A-N+8)个质子,所以Wg 它的氧化物中所含质子的物质的量为$\frac{Wg}{(A+16)g/mol}$×(A-N+8)=$\frac{W}{A+16}$(A-N+8),
故选A.
点评 本题考查物质的量有关计算以及质子数、中子数、质量数之间的关系,难度不大,注意质量数在数值上等于其近似相对原子质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,30s后,水蒸气的物质的量增加了4.5mol,则此反应的平均速率v (X)可表示为( )
| A. | v(NH3)=0.010mol•L-1•s-1 | B. | v (O2)=0.010mol•L-1•s-1 | ||
| C. | v (NO)=0.15mol•L-1•s-1 | D. | v (H2O)=0.15mol•L-1•s-1 |
8.下列化学式只能表示一种物质的是( )
| A. | C3H6 | B. | C2H6O | C. | C6H6 | D. | CH2Cl2 |
5.下列关于价电子构型为4s24p4的基态原子描述正确的是( )
| A. | 它的元素名称为锡 | B. | 它的核外电子排布式为[Ar]4s24p4 | ||
| C. | 它的第一电离能小于As | D. | 其外围电子排布图为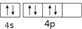 |
2.下列各组有机物的鉴别(括号内为鉴别试剂)不合理的是( )
| A. | 苯、甲苯、溴乙烷(酸性高锰酸钾溶液) | B. | 乙醇、乙醛、乙酸(新制Cu(OH)2) | ||
| C. | 苯、乙醇、四氯化碳(溴水) | D. | 苯、己烷、苯酚溶液(浓溴水) |
7.下列离子方程式书写正确的是( )
| A. | 单质钠放入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | 二氧化硅溶于NaOH溶液:SiO2+2OH-═SiO32-+H2O | |
| C. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
 .
.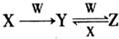 已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.
已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.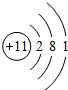 ,用电子式写出C和E形成化合物的过程
,用电子式写出C和E形成化合物的过程 ,用电子式写出A和B形成化合物的过程
,用电子式写出A和B形成化合物的过程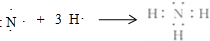 .
.